我委拟修订聚乙烯醇药用辅料标准,为确保标准的科学性、合理性和适用性,现将拟制定(修订)的药用辅料标准公示征求社会

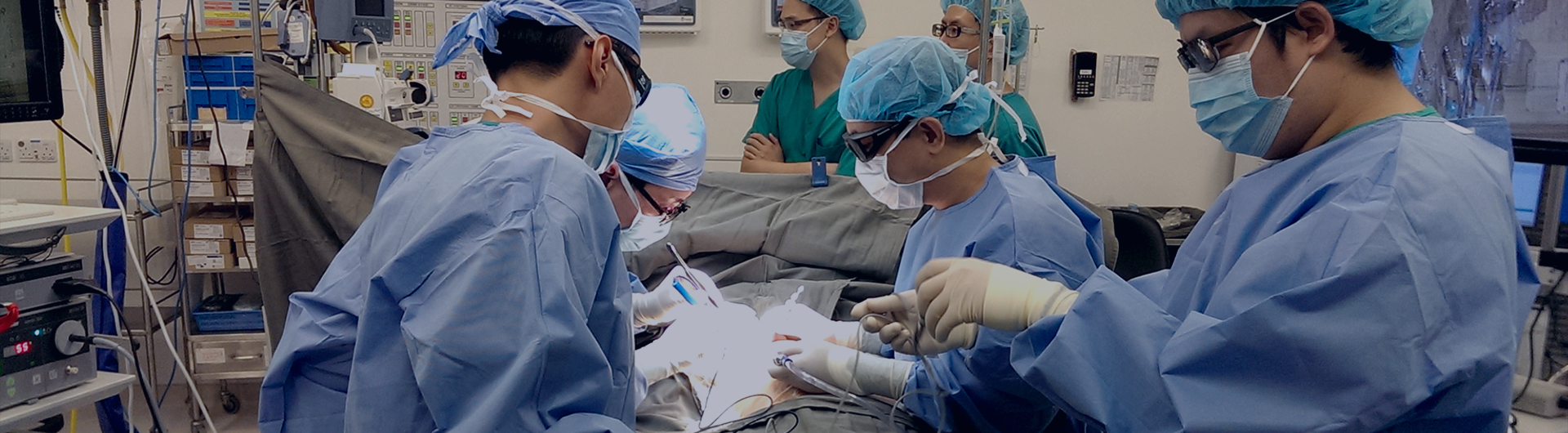
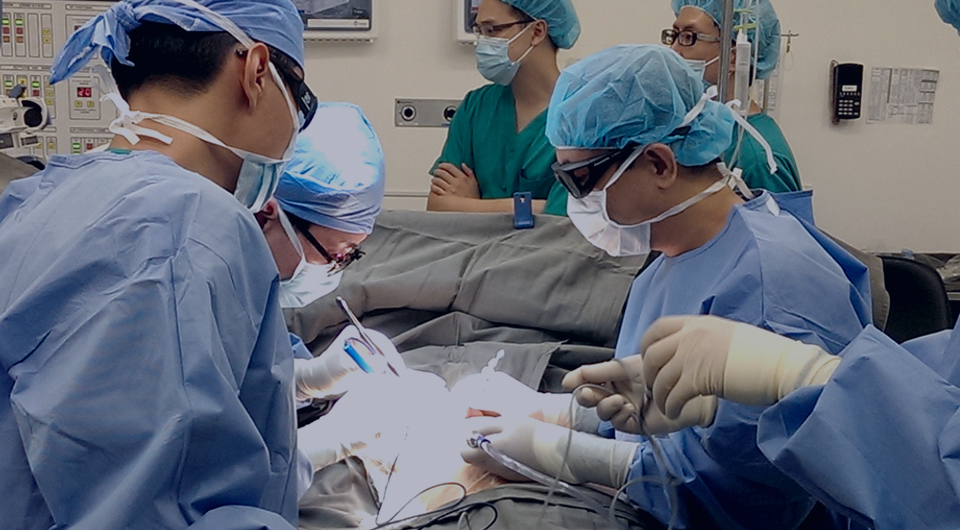
 临床难题及解决方案
临床难题及解决方案
抗体偶联药物(Antibody–Drug Conjugates,ADC)目前是抗肿瘤新药研发热点之一,尤其是在肿瘤治疗领域,ADC的药物研发持续增长。
为了对ADC类抗肿瘤药物的临床研发中,需要特殊关注的问题提出建议,并指导企业更为科学地进行ADC的临床研发,药审中心组织制定了《抗肿
瘤抗体偶联药物临床研发技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管
〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2023年4月6日
为进一步鼓励创新,药审中心组织制定了《药审中心加快创新药上市许可申请审评工作规范(试行)》,经国家药品监督管理局审核同意,现予发
布,自发布之日起实施。
国家药监局药审中心
2023年3月31日
为指导企业提高儿科人群药物研发效率,药审中心组织制定了《生理药代动力学模型在儿科人群药物研发中应用的技术指导原则》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发
布,自发布之日起施行。
特此通告。
国家药监局药审中心
2023年3月27日
为鼓励创新,加快新药研发,提高申请人和监管机构沟通交流的质量和效率,在国家药品监督管理局的部署下,药审中心组织制定了《化学药品
创新药Ⅲ期临床试验前会议药学共性问题及相关技术要求(试行)》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现
予发布,自发布之日起施行。
特此通告。
附件:化学药品创新药Ⅲ期临床试验前会议药学共性问题及相关技术要求(试行)
国家药监局药审中心
2023年3月22日
为了对儿童抗肿瘤新药的临床研发提供思路和技术建议,药审中心组织撰写了《儿童抗肿瘤药物临床研发技术指导原则》(见附件)。根据《国
家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发
布之日起施行。
特此通告。
国家药监局药审中心
2023年3月22日
根据《药品上市后变更管理办法(试行)》,为明确境外生产药品转移至境内生产的药品上市申报相关程序及技术要求,药审中心起草了《已上市
境外生产药品转移至境内生产的药品上市注册申请申报资料要求(化学药品)(征求意见稿)》。现在中心网站予以公示,以广泛听取各界意见和建
议。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个月。
您的反馈意见请发到以下联系人的邮箱:
联系人:王磊、龚青
邮箱:wangl@cde.org.cn,gongq@cde.org.cn
感谢您的参与和大力支持!
附件:1. 已上市境外生产药品转移至境内生产的药品上市注册申请申报资料要求(化学药品)(征求意见稿)
2. 《已上市境外生产药品转移至境内生产的药品上市注册申请申报资料要求(化学药品)(征求意见稿)》政策解读
3. 《已上市境外生产药品转移至境内生产的药品上市注册申请申报资料要求(化学药品)(征求意见稿)》起草说明
4. 《已上市境外生产药品转移至境内生产的药品上市注册申请申报资料要求(化学药品)(征求意见稿)》征求意见反馈表
药品审评中心
2023年3月23日
为规范和指导病毒去除/灭活工艺平台验证临床试验阶段的申报和评价,我中心在前期调研的基础上,结合国内外相关法规和技术要求,以及基
于当前病毒清除验证的经验积累和科学认知,形成了《治疗用重组生物技术产品病毒去除/灭活工艺平台验证技术指导原则(征求意见稿)》。现通
过中心网站向社会公开征求意见,诚挚欢迎社会各界对征求意见稿提出宝贵意见和建议,请在征求意见反馈表填写具体信息,并通过邮件反馈我们。
感谢您的参与和支持!
征求意见时限为自发布之日起一个月。
联系人:胡莹莹,Email:huyy@cde.org.cn;
赛文博,Email:saiwb@cde.org.cn;
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2023年3月22日
为鼓励新药研发,在国家药品监督管理局的部署下,药审中心组织制定了《治疗卵巢癌新药临床研发技术指导原则(试行)》(见附件)。根据
《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,
自发布之日起施行。
特此通告。
附件:治疗卵巢癌新药临床研发技术指导原则(试行)
国家药监局药审中心
2023年3月20日
为加强药品说明书及标签的规范管理,促进企业有序开展起草和完善说明书及标签中药学信息的相关工作,在国家药品监督管理局
的部署下,药审中心组织制定了《化学药品说明书及标签药学相关信息撰写指导原则(试行)》(见附件)。根据《国家药监局综合司
关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布
之日起施行。
特此通告。
国家药监局药审中心
2023年3月20日
为指导企业研发,统一审评尺度,助力ICH《Q13:原料药和制剂的连续制造》指导原则在国内实施,在国家药品监督管理局的部署下,药审中
心组织起草了《化药口服固体制剂连续制造技术指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通
知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2023年3月20日
为推动新修订的ICH指导原则在国内的平稳落地实施,我中心拟定了《<M10:生物分析方法验证和研究样品分析>问答文件和常见问题解答文件
的实施建议》,同时组织翻译了M10问答文件和常见问题解答文件的中文版。现对以上实施建议和中文版公开征求意见,为期1个月。
如有修改意见,请反馈至联系人电子邮箱:gkzhqyj@cde.org.cn。
国家药品监督管理局药品审评中心
2023年3月17日
阿片类药物的滥用已在全球范围内成为日益严重的公共卫生问题。为鼓励开发具有防滥用特性的阿片类口服固体仿制药,提供研究与评价的药学
技术标准,在国家药品监督管理局的部署下,药审中心组织制定了《阿片类口服固体仿制药防滥用药学研究技术指导原则(试行)》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现
予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2023年3月16日
根据现行《药品注册管理办法》《药物临床试验质量管理规范》和《药物警戒质量管理规范》,为推进临床试验期间安全信息汇总分析与风险评
估工作,在国家药品监督管理局的部署下,药审中心组织制定了《药物临床试验期间安全性信息汇总分析和报告指导原则(试行)》(见附件)。根
据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发
布,自发布之日起施行。
特此通告。
附件:药物临床试验期间安全性信息汇总分析和报告指导原则(试行)
国家药监局药审中心
2023年3月17日
复方药物是指含有两种或两种以上活性成份的药物,其临床研发具有特殊性。为了科学引导企业合理开发复方药物,进一步明确技术标准,药审
中心组织制定了《化药复方药物临床试验技术指导原则》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现
予发布,自发布之日起施行。
特此通告。
附件:化药复方药物临床试验技术指导原则
国家药监局药审中心
2023年3月17日
根据国家局2019年3月28日发布的《关于发布化学仿制药参比制剂遴选与确定程序的公告》(2019年第25号),我中心组织遴选了第六十八批
参比制剂(见附件),现予以公示征求意见。
公示期间,请通过参比制剂遴选申请平台下“参比制剂存疑品种申请”模块向药审中心进行反馈,为更好服务申请人,反馈意见请提供充分依据
和论证材料,反馈材料应加盖单位公章,并提供真实姓名和联系方式。
公示期限:2023年3月15日~2023年3月28日(10个工作日)。
国家药品监督管理局药品审评中心
2023年3月15日
为阐明当前对单臂临床试验用于支持抗肿瘤药上市申请的适用性的科学认识,指导企业在完成早期研究后,更好地评估是否适合开展单臂临床试
验作为关键临床研究,以支持后续的上市申请,在国家药品监督管理局的部署下,药审中心组织制定了《单臂临床试验用于支持抗肿瘤药上市申请的
适用性技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国
家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
附件:单臂临床试验用于支持抗肿瘤药上市申请的适用性技术指导原则
国家药监局药审中心
2023年3月14日
为指导我国前列腺癌领域抗肿瘤药物的临床研发,提供可参考的技术标准,在国家药品监督管理局的部署下,药审中心组织制定了《晚
期前列腺癌临床试验终点技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管
〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
附件:晚期前列腺癌临床试验终点技术指导原则
国家药监局药审中心
2023年3月14日
药审中心在中国药品监管科学行动计划第一批重点项目“纳米类药物安全性评价及质量控制研究”的研究中,已起草并发布了纳米药物
质量控制、非临床药代动力学、非临床安全性评价研究三个技术指导原则。但是,不同类型的纳米药物具有其不同的特性,需要探索细化不
同类型纳米药物的研究策略。纳米药物中很重要的一类为载体类纳米药物,其中粒径处于纳米级的脂质体药物是一类具有代表性的载体类纳
米药物。
为了更科学地引导药物研发,探索建立脂质体药物监管标准,药审中心在中国药品监管科学行动计划第二批重点项目“纳米类创新药
物、医疗器械安全性有效性和质量控制评价研究”(药物部分)的研究中,针对脂质体药物进行重点研究,通过前期广泛调研,在项目子课
题组撰写初稿的基础上,药审中心撰写形成了《脂质体药物质量控制研究技术指导原则》《脂质体药物非临床药代动力学研究技术指导原
则》征求意见稿,现公开征求意见和建议。
我们诚挚地期待社会各界对征求意见稿提出宝贵意见并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个月。
您的反馈意见请发到以下联系人的邮箱:
质量控制指导原则:
联系人:章俊麟zhangjl@cde.org.cn,石勇平 shiyp@cde.org.cn
非临床药代指导原则:
联系人:黄芳华huangfh@cde.org.cn,付淑军fushj@cde.org.cn
感谢您的参与和大力支持!
国家药品监督管理局药品审评中心
2023年3月14日
为进一步规范药物非临床研究质量管理规范认证和监督管理工作,国家药品监督管理局组织修订了《药物非临床研究质量管理规范认证 管理办法》,现予发布。自2023年7月1日起施行。
特此公告。
国家药监局
2023年1月19日
为了规范和指导化学仿制药溶液型滴眼剂的药学研发,在国家药品监督管理局的部署下,药审中心组织制定了《化学药品仿制药溶
液型滴眼剂药学研究技术指导原则》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局
审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2023年2月6日
为进一步指导吸入制剂现场检查工作,帮助检查员识别吸入制剂的风险控制点,提高现场检查质量,核查中心组织制定了《吸入制剂现场检查指南》。
经国家药品监督管理局同意,现予发布。
特此通告。
国家药监局核查中心
2023年3月6日
为指导和规范药品共线生产管理,最大程度降低共线生产产品间的污染、交叉污染,保证药品安全、有效和质量可控,确保患者用药安全,核查中心组织制定了《药品共线生产质量风险管理指南》。
经国家药品监督管理局同意,现予发布。
特此通告。
国家药监局核查中心
2023年3月6日
一、《中药注册管理专门规定》(以下简称《专门规定》)的制定背景是什么?
自1985年《药品管理法》实施以来,在不同历史阶段,国家药品监督管理部门针对中药的特点和研制规律,曾先后出台过《中药审批办法》《<新药审批办法>有关中药问题的补充规定和说明》等文件,不断探索完善对中药审批工作的管理。2008年,原国家食药监局发布了《中药注册管理补充规定》(以下简称《补充规定》),至今已十余年。《补充规定》的实施对中医药事业的发展起到了积极的推动作用。
近年来,习近平总书记多次对中医药工作作出重要指示,《药品管理法》《中医药法》的修订颁布,《中共中央 国务院关于促进中医药传承创新发展的意见》《国务院办公厅关于加快中医药特色发展的若干政策措施》陆续发布,全国中医药大会召开,我国中医药传承创新发展迈进新时代。2018年机构改革后,国家药监局党组高度重视中药监管工作,研究部署对《补充规定》作进一步修订完善。为全面落实《中共中央 国务院关于促进中医药传承创新发展的意见》,并与新修订《药品管理法》《药品注册管理办法》有机衔接,经研究决定对《补充规定》进行修订,并将《补充规定》的名称修改为《专门规定》。
二、《专门规定》的主要内容是什么?
《专门规定》共十一章,共82条。主要内容分为总则、中药注册分类与上市审批、人用经验证据的合理应用、中药创新药、中药改良型新药、古代经典名方中药复方制剂、同名同方药、上市后变更、中药注册标准、药品名称和说明书、附则等。其中:
第一章总则,共10条。强调传承与创新并重,坚持以临床价值为导向、中医药理论指导,注重临床实践,改革、完善审评证据体系和疗效结局指标;建立符合中药特点的安全性评价要求,强化中药研制全过程的质量控制,保障中药资源可持续利用。
第二章中药注册分类与上市审批,共6条。明确中药注册分类、研制路径和模式,建立适合中药研制情形的简化审批、优先审批、附条件审批、特别审批的相应规定。
第三章人用经验证据的合理应用,共11条。明确了中药人用经验的具体内涵,以及作为支持中药安全性、有效性证据的合规性和药学研究要求;明确了合理使用人用经验证据支持注册申请,合理豁免非临床安全性研究及部分临床试验的情形;引入真实世界证据作为支持产品上市的依据;对医疗机构中药制剂应用人用经验的情形进行明确。
第四章中药创新药,共13条。根据中药特点分别规定了临床、药学及药理毒理方面的相应要求,涉及明确中药复方组方要求,新药材及其制剂、提取物及其制剂研究基本原则和要求等。
第五章中药改良型新药,共7条。明确改良型新药研发的基本原则,并针对改剂型、改变给药途径、增加功能主治、改变工艺或辅料等引起药用物质基础或药物吸收、利用明显改变等改良型新药情形,分别提出研制要求。
第六章古代经典名方中药复方制剂,共6条。明确了古代经典名方制剂的注册管理总体要求、研制基本要求、审评模式,以及该类制剂上市后的研究要求。
第七章同名同方药,共6条。明确了同名同方药的研制基本原则,规定了对照同名同方药的选择要求,以及同名同方药开展临床试验以及豁免临床试验的条件。
第八章上市后变更,共8条。提出中药上市后变更的总体要求;明确了变更规格、生产工艺及辅料、适用人群、用法用量、处方药味等常见变更情形的研制要求;明确替代或减去国家药品标准处方中的毒性药味或处于濒危状态药味、将处方中按新药批准的提取物由外购变更为自行提取、删除主治或者适用人群范围等特殊变更情形的研制要求。
第九章中药注册标准,共4条。明确中药注册标准的研制目标,支持探索建立整体质量控制方法和持续完善中药质量标准体系;明确企业内控标准与注册标准的关系。
第十章药品名称和说明书,共5条。明确中药通用名称的命名要求,对已上市中药的说明书完善提出了要求。对含毒性中药饮片的中药、主治为证候的中药复方制剂以及来源于古代经典名方中药复方制剂的说明书均作出了针对性的有关要求。
第十一章附则,共6条。主要包括天然药物、境外已上市而境内未上市产品、中药注射剂等的研制要求,以及医疗机构中药制剂的注册管理有关规定。明确《专门规定》施行日期等。
三、《专门规定》的定位
《专门规定》是在《补充规定》实施基础上,充分吸纳药品审评审批制度改革成熟经验,结合疫情防控中药成果转化实践探索,借鉴国内外药品监管科学研究成果,全方位、系统地构建了中药注册管理体系。《专门规定》是介于《药品注册管理办法》和系列药品研制技术指导原则之间的规范性文件,内容既涉及中药注册方面的行政管理事务,又涉及中药审评审批专业技术内容。《专门规定》对中药人用经验的合理应用以及中药创新药、中药改良型新药、古代经典名方中药复方制剂、同名同方药等注册分类的研制原则和技术要求进行了明确。《专门规定》通过必要的技术要求表述,进一步落实加快推进完善中医药理论、人用经验和临床试验相结合(以下简称“三结合”)的中药审评证据体系,体现中药注册管理的新理念和改革举措,并加强了对中药研制的指导,具有较强的实操性。
四、《专门规定》主要特点
(一)将药品的基本要求与中药特殊性有机结合
中药与其他药品的共同点是以临床价值为导向,用于人体疾病的预防、治疗、诊断,而不同点在于中药具有丰富的临床人用经验,中药的人用经验蕴含着重要的有效性和安全性信息,“临床-实验室-临床”是中药新药研发的主要路径和特点。因此,《专门规定》遵循中药研制规律和特点,不断强化“以临床价值为导向、重视人用经验、全过程质量控制”等研制理念,将中药的生产工艺、质量标准、药效学、毒理学、临床研究等各研制内容有机结合,结合药品安全性、有效性、质量可控性的基本要求,建立起兼顾药品基本要求,具有中药特点的审评审批体系。
(二)辩证处理好中药传承与创新的关系
推动中药高质量发展,要善于传承、勇于创新。中医药具有历史悠久的临床实践,为中药研发提供了宝贵经验和指导理论;同时,中药的创新发展,也需要充分运用现代科学技术。中药的传承与创新是相互统一、相互依存、相互促进的关系。《专门规定》明确中药新药研制应当注重体现中医药原创思维及整体观,鼓励运用传统中药研究方法和现代科学技术研究、开发中药;支持研制基于古代经典名方、名老中医经验方、医疗机构中药制剂等具有丰富中医临床实践经验的中药新药。同时,《专门规定》鼓励应用新兴科学和技术研究阐释中药的作用机理,鼓励将真实世界研究、新型生物标志物、替代终点决策、以患者为中心的药物研发、适应性设计、富集设计等用于中药疗效评价,在此基础上推动中药新药研制创新。
(三)充分尊重中药人用经验
中医药学极其注重临床实践,中医药具有悠久的人用经验和数据,人用经验反映了中药的实践性特点。中药研制一般具有“源于临床,用于临床”的特点,中药新药在上市前多数已有一定的人用经验。将已有的中药人用经验整合入中药的审评证据体系,长期以来一直是业界的呼声,也是药品监管部门积极探索构建符合中药特点的审评技术评价体系的切入点。2021年以来,国家药监局加快了构建“三结合”的中药审评证据体系步伐。《专门规定》充分重视“人用经验”对中药安全性、有效性的支撑,设立专章,对中药人用经验的具体内涵,作为支持中药安全性、有效性证据的合规性、药学研究要求,以及人用经验证据支持注册申请的情形等进行明确,促进了“三结合”审评证据体系的加快建立和完善;同时,还明确注册申请人可根据中药人用经验对中药安全性、有效性的支持程度和不同情形,在研制时可选择不同的临床研究路径,将极大地激发中药新药研制的活力。
(四)系统阐释了中药注册分类研制原则要求
目前,调整后的中药注册分类尊重中药研发规律、突出中药特色,鼓励具有中医药特点的中药复方制剂创新,注重以临床价值为导向,不再以物质基础作为划分注册类别的依据。《专门规定》按照调整后的中药注册分类(中药创新药、中药改良型新药、古代经典名方中药复方制剂及同名同方药等)的不同特点,分章节系统阐释。依法简化古代经典名方中药复方制剂审批,构建与制剂特点相适应的审评模式,促进古代经典名方中药复方制剂研发。
(五)明确了中药疗效评价指标的多元性
《专门规定》基于中医药在临床中发挥的作用和特点,明确了中药的疗效评价应当结合中医药临床治疗特点,确定与中药临床定位相适应、体现其作用特点和优势的疗效指标;挖掘中医药临床价值,列举了可作为中药疗效评价的8种情形(对疾病痊愈或者延缓发展、病情或者症状改善、患者与疾病相关的机体功能或者生存质量改善、与化学药品等合用增效减毒或者减少毒副作用明显的化学药品使用剂量等情形),丰富了以临床价值为导向的多元化中药临床疗效评价方法,促进了中医药独特的评价方法与体系的建立,为中药新药研制拓展思路。
根据国家局2019年3月28日发布的《关于发布化学仿制药参比制剂遴选与确定程序的公告》(2019年第25号),我中心组织遴选了第六十七批参比制剂(见附件),现予以公示征求意见。
公示期间,请通过参比制剂遴选申请平台下“参比制剂存疑品种申请”模块向药审中心进行反馈,为更好服务申请人,反馈意见请提供充分依据和论证材料,反馈材料应加盖单位公章,并提供真实姓名和联系方式。
公示期限:2023年2月21日~2023年3月6日(10个工作日)。
国家药品监督管理局药品审评中心
2023年2月21日
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2023年2月17日
特此通告。
国家药监局药审中心
2023年2月17日
为了规范和指导化学仿制药溶液型滴眼剂的药学研发,在国家药品监督管理局的部署下,药审中心组织制定了《化学药品仿制药溶液型滴眼剂药学研究技术指导原则》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2023年2月6日
为进一步加强质量风险管理在产品质量控制中的应用,提高非无菌化学药品及原辅料微生物限度标准制定的科学性及合理性,在国家药品监督管理局的部署下,药审中心组织制定了《非无菌化学药品及原辅料微生物限度研究技术指导原则(试行)》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予以发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2023年2月17日
特此通告。
国家药监局药审中心
2023年2月6日
特此通告。
国家药监局药审中心
2023年2月6日
为了指导申办者科学合理的设计真实世界研究,明确真实世界研究方案撰写的技术要求,药审中心组织制定了《药物真实世界研究设计与方案框架指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2023年2月6日
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2023年2月6日
特此通告。
国家药监局药审中心
2023年2月10日
为规范和指导原发性胆汁性胆管炎(PBC)治疗药物临床试验,提供可参考的技术规范,在国家药品监督管理局的部署下,药审中心组织制定了《原发性胆汁性胆管炎治疗药物临床试验技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2023年2月10日
为规范和指导溶瘤病毒产品的药学研发、生产和注册,在国家药品监督管理局的部署下,药审中心组织制定了《溶瘤病毒产品药学研究与评价技术指导原则(试行)》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2023年2月10日
M11指导原则草案的英文原文和中文译文见附件,现就该指导原则内容及中文译文向社会公开征求意见。
社会各界如有相关建议,请于2023年3月15日前通过联系人电子邮件反馈我中心。
联系人:赵建中、何春俐
邮箱:zhaojzh@cde.org.cn, hechl@cde.org.cn
国家药品监督管理局药品审评中心
2023年1月6日
ICH委员会组织专家组对ICH指导原则Q9(Quality Risk Management)进行了修订,修订后的ICH指导原则《Q9(R1):质量风险管理》已
于2023年1月18日进入第4阶段。我中心组织翻译,形成了中文翻译稿。
为准确表达原意,现就该中文翻译稿向社会公开征求意见。请于2023年2月28日前通过电子邮箱反馈我中心。
联系人:杜婧
邮 箱:gmp-cfdi@cfdi.org.cn
国家药品监督管理局
食品药品审核查验中心
2023年1月28日
为更好地落实《国家药监局关于实施药品注册申请电子申报的公告》(2022年第110号)要求,统一eCTD申报资料和电子申报资料关于文件大小的有关要求,药品审评中心对《eCTD实施指南V1.0》(以下简称《实施指南》)及《eCTD验证标准V1.0》(以下简称《验证标准》)进行了修订,形成征求意见稿。
修订内容主要包括:
一、删除《实施指南》2.8章节关于纸质资料的递交要求;
二、删除《实施指南》4.1.2章节和附件说明函中关于纸质资料的相关内容,包括“关于纸质资料与eCTD申报资料内容一致的承诺”和“关于按规定时限一次性提交全部纸质申报资料的承诺;
三、修改《实施指南》7.6章节关于文件大小的要求,将单个PDF文件应控制在500MB以内修改为200MB以内;
四、对《验证标准》相对应部分进行了修订。
现向社会公开征求意见,征求意见时限为自发布之日起1个月。请将反馈意见发送到以下联系人的邮箱,感谢您的参与和大力支持。
联系人:李海玲
联系方式:lihl@cde.org.cn
国家药品监督管理局药品审评中心
2023年1月29日
为鼓励抗肿瘤新药研发,在国家药品监督管理局的部署下,药审中心组织制定了《慢性淋巴细胞白血病新药临床研发技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
附件:慢性淋巴细胞白血病新药临床研发技术指导原则
国家药监局药审中心
2023年1月6日
为推动新修订的ICH指导原则在国内的平稳落地实施,我中心拟定了《E19:在特定的上市前后期或上市后临床试验中选择性收集安全
性数据》实施建议,同时组织翻译中文版。现对E19实施建议和中文版公开征求意见,为期1个月。
如有修改意见,请反馈至联系人电子邮箱:gkzhqyj@cde.org.cn。
附件:1.E19实施建议
2.E19中文版
3.E19英文版
国家药品监督管理局药品审评中心
2023年1月6日
公示期间,请通过参比制剂遴选申请平台下“参比制剂存疑品种申请”模块向药审中心进行反馈,为更好服务申请人,反馈意见请提供充分依据和论证材料,反馈材料应加盖单位公章,并提供真实姓名和联系方式。
公示期限:2023年1月9日~2023年1月20日(10个工作日)。
国家药品监督管理局药品审评中心
2023年1月09日
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个月。
您的反馈意见请发到以下联系人的邮箱:
联系人:周贝,zhb@cde.org.cn
杨娜,yangn@cde.org.cn
感谢您的参与和大力支持!
药品审评中心
2023年1月6日
随着病程的延长,2型糖尿病患者单药治疗失效的几率逐渐增加,往往需要采用联合治疗才能使血糖得到良好控制。联合治疗是糖尿病患者控制血糖必不可少的重要手段,糖尿病药物复方制剂的研发上市为糖尿病的治疗提供了更多的药物治疗手段。
本指导原则在《复方药物临床试验技术指导原则》的基础上,基于糖尿病疾病特征、治疗理念和临床实践情况,结合2型糖尿病复方降糖药物的特点以及研发需关注的问题提供建议。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起一个月。
您的反馈意见请发到以下联系人的邮箱:
联系人:张杰 李远红
联系方式: zhangj @cde.org.cn liyh@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2023年1月3日
为了向申办者提供在临床试验中正确设计和实施盲法的指导性建议,药审中心在国家药品监督管理局的部署下,组织制定了《药物临床
试验盲法指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9
号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年12月30日
根据国家局2019年3月28日发布的《关于发布化学仿制药参比制剂遴选与确定程序的公告》(2019年第25号),我中心组织遴选了第
六十五批参比制剂(见附件),现予以公示征求意见。
公示期间,请通过参比制剂遴选申请平台下“参比制剂存疑品种申请”模块向药审中心进行反馈,为更好服务申请人,反馈意见请提供
充分依据和论证材料,反馈材料应加盖单位公章,并提供真实姓名和联系方式。
公示期限:2022年12月29日~2023年1月11日(10个工作日)。
国家药品监督管理局药品审评中心
2022年12月29日
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年12月26日
非阿片类术后镇痛领域进入临床试验阶段的创新药和改良型新药逐年增多,为科学引导和规范我国此类药物的临床研发,药品审评中心
组织撰写了《非阿片类术后镇痛新药临床试验设计技术指导原则》,并形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:李强
联系方式:liq@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心 2022年12月22日
为推动新修订的ICH指导原则在国内的平稳落地实施,我中心拟定了《S1B(R1):致癌性研究》实施建议,同时组织翻译中文版。现对
S1B(R1)实施建议和中文版公开征求意见,为期1个月。
如有修改意见,请反馈至联系人电子邮箱:gkzhqyj@cde.org.cn
国家药品监督管理局药品审评中心 2022年12月22日
免疫原性是预防用疫苗评价的重要手段之一,通过免疫原性桥接临床试验(简称免疫桥接试验),比较疫苗在不同条件下引起的免疫应
答和安全性特征,可推测和借鉴疫苗的安全有效性。免疫桥接试验有特定的适用领域和设计特点,为指导申请人科学和合理的开展规范的免
疫桥接试验,我中心撰写了《预防用疫苗免疫原性桥接临床试验技术指导原则(征求意见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:殷霄,刘波
联系方式: yinx@cde.org.cn,liub@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心 2022年12月21日
为推动构建中医药理论、人用经验和临床试验相结合的中药注册审评证据体系,探索符合中医药特点的疗效评价标准,在国家药品监督
管理局的部署下,药审中心组织制定了《中药新药用于慢性胃炎的临床疗效评价技术指导原则(试行)》《中药新药用于胃食管反流病的临
床疗效评价技术指导原则(试行)》。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)
要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年12月19日
对疾病自然史的深入研究和全面了解,是人类认识疾病,并对疾病进行诊断、治疗以及开展药物研发的基础。近年来,随着医药行业对
罕见疾病治疗药物研发热情不断增加,罕见疾病的疾病自然史研究显得尤为重要。
为推动和规范我国罕见疾病的疾病自然史研究,药审中心相关适应症小组组织撰写了《罕见疾病药物开发中疾病自然史研究指导原则
(征求意见稿)》。本指导原则旨在结合我国罕见疾病研究现状,提出符合我国国情的罕见疾病药物开发中疾病自然史研究的考虑要点。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:唐凌,赵伯媛
联系方式:tangl@cde.org.cn,zhaoby@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年12月21日
为进一步规范和加强药品标准管理,保障药品安全性、有效性和质量可控性,国家药监局组织起草了《药品标准管
理办法(征求意见稿)》,现向社会公开征求意见。
公开征求意见的时间为2022年12月15日至2023年1月14日。有关单位和个人可以将意见反馈至
yhzcszhc@nmpa. gov.cn。请在电子邮件主题注明“药品标准管理办法有关意见反馈”。
附件:
1.药品标准管理办法(征求意见稿)
2.《药品标准管理办法》起草说明
3.《药品标准管理办法(征求意见稿)》意见反馈表
国家药监局综合司
2022年12月14日



为进一步规范和指导慢性肾脏病治疗药物临床试验,提供可参考的技术规范,我中心起草了《慢性肾脏病治疗药物临床试验技术指导原
则》,经中心内部讨论,已形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:王水强,李杰静
联系方式:wangshq @cde.org.cn;lijj@ cde.org.cn
感谢您的参与和大力支持。
药品审评中心
2022年11月16日
为推动构建中医药理论、人用经验和临床试验相结合的中药注册审评证据体系,引导申请人按照“三结合”注册审评证据体系研发符合
中医药治疗优势和特点的、与恶性肿瘤治疗相关的中药新药复方制剂,药审中心起草了《与恶性肿瘤治疗相关中药新药复方制剂临床研发技
术指导原则(征求意见稿)》,经中心内部讨论并组织学术界专家研讨,已形成征求意见稿。现在中心网站予以公示,以广泛听取各界意见
和建议。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
联系人:薛斐然 xuefr@cde.org.cn,安娜anna@cde.org.cn。
感谢您的大力支持!
药品审评中心
2022年11月17日
按照《国家药监局关于实施药品注册申请电子申报的公告》(2022年第110号)要求,自2023年1月1日起,申请人提交的国家药监
局审评审批药品注册申请以及审评过程中补充资料等,调整为以电子形式提交申报资料,现就电子申报具体要求通知如下:
一、电子申报资料准备
申请人应当按照现行法规、申报资料电子光盘技术要求及药品注册申请电子文档结构等相关要求准备电子申报资料(含承诺书),并
将光盘提交至药审中心提出药品注册申请。申请人或注册代理机构需对电子申报资料进行电子签章,电子签章的申领和使用详见药审中心
网站“申请人之窗”栏目“CA直通车”。
光盘盒封面及档案袋封面要求详见申报资料电子光盘技术要求(附件1)。
二、电子申报资料接收与受理
(一)药审中心收到申请人提交的光盘后,对可正常读取、通过电子签章校验且未发现计算机病毒的光盘进行接收;如光盘损坏、光
盘数据无法读取、电子签章校验不通过或发现计算机病毒的,药审中心将及时与申请人进行沟通并提醒重新递交,原光盘将按照销毁程序
处理。
(二)药审中心在5个工作日内对接收的申报资料进行受理形式审查。受理行政许可电子文书均由“药品业务应用系统”、“药品
eCTD注册系统”推送并以短信提醒,申请人可即时查询和打印,药审中心不再邮寄受理行政许可纸质文书。
(三)对于申请材料不齐全或者不符合法定形式需要补正的,或不符合要求需要不予受理的,或审评过程中补充资料等不符合《药品
审评中心补充资料工作程序(试行)》等相关接收要求的,申报资料光盘由药审中心按程序进行销毁处理,不再退回申请人,请申请人留
好备份。
三、其他要求
(一)关于光盘整理
申请人需按本通知要求提交1套完整的电子申报资料光盘(含临床试验数据库,如适用)供审评使用。
同时,除药物临床试验申请、境外生产药品再注册申请及直接行政审批的补充申请等不涉及核查的申请外,申请人还需同时提交1套
完整的电子申报资料光盘(含临床试验数据库,如适用)供核查使用。涉及通用名称核准资料、临床试验数据库资料、需非处方药适宜性
审查和说明书审核的等,相关资料需另外再单独准备1套光盘。
后续随着信息化工作逐步推进,药审中心将及时调整相关要求。
(二)关于审评过程中资料提交要求
实施电子申报前,申请人已提交药品注册申请且已受理的,审评过程中补充资料等仍采用纸质申报资料形式进行递交。
实施电子申报后受理的药品注册申请,审评过程中补充资料等采用电子申报资料形式进行递交。
(三)关于“申请人之窗”提交资料要求
药品注册申请受理后5个工作日内,申请人需通过药审中心网站“申请人之窗”栏目上传药学、非临床及临床综述等申报资料WORD
文档并确保文档内容独立完整,满足复制、检索等要求。
(四)关于原料药、药用辅料和药包材登记资料
原料药登记资料应采用PDF格式文件进行整理,电子签章等相关要求应符合申报资料电子光盘技术要求。鼓励药用辅料和药包材登记
资料参照执行。
附件:1. 申报资料电子光盘技术要求
2. 药品注册申请电子文档结构
3. 承诺书
国家药监局药审中心
2022年12月2日
为进一步指导我国新药研发,加快新药研发上市进程,加强与非临床机构、研发企业的沟通交流,提升我国新药研发水平和效率,药审
中心定于2022年12月8日举办“新药非临床研究技术指导原则”线上培训。现将有关事项通知如下:
一、会议时间
2022年12月8日13:30-18:00
二、会议方式
采用在线平台进行线上直播。
三、参加人员
面向全社会公开,新药研发相关非临床机构、制药企业人员。
四、主要内容
介绍基因治疗产品、基因修饰细胞治疗产品、纳米药物、放射性体内诊断药物非临床研究技术指导原则等相关内容,具体议程详见附
件。
五、报名注册
1. 此次培训不收取报名费,参会人员需要扫描二维码进入注册即可。名额有限,报完为止。
电脑端链接:https://wx.vzan.com/live/pc/expo/index/1773?zbid=1772732231
2. 请参与培训的学员,注册后通过问题收集页面,提交需要讲者回复的问题,讲者授课后进行答疑与研讨。
ICH指导原则《Q5A(R2):来源于人或动物细胞系生物技术产品的病毒安全性评价》现进入第3阶段征求意见。按照ICH相关章程要求,
ICH监管机构成员需收集本地区关于第2b阶段指导原则初稿的意见并反馈ICH。
Q5A(R2)原文和中文译文见附件,现就该指导原则内容及中文译文翻译稿向社会公开征求意见。
社会各界如有意见(填写附件3),请于2023年1月20日前通过电子邮箱反馈我中心。
联系人:赛文博、于鹏丽
邮 箱:saiwb@cde.org.cn;yupl@cde.org.cn
附件:1.【英文】Q5A(R2):来源于人或动物细胞系生物技术产品的病毒安全性评价(初稿)
2.【中文】Q5A(R2):来源于人或动物细胞系生物技术产品的病毒安全性评价(初稿)
3.【模板】征求意见反馈表
国家药品监督管理局药品审评中心
2022年11月28日
为不断丰富完善仿制药个药指导原则并持续推进一致性评价工作,进一步指导注射用两性霉素B脂质体生物等效性研究的实施和评价,
药审中心组织起草了《注射用两性霉素B脂质体生物等效性研究技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指
导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年11月21日
为不断丰富完善仿制药个药指导原则并持续推进一致性评价工作,进一步指导他达拉非片生物等效性研究的实施和评价,药审中心组织
起草了《他达拉非片生物等效性研究技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》
(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
附件:他达拉非片生物等效性研究技术指导原则
国家药监局药审中心
2022年11月21日
为不断丰富完善仿制药个药指导原则并持续推进一致性评价工作,进一步指导注射用两性霉素B脂质体生物等效性研究的实施和评价,
药审中心组织起草了《注射用两性霉素B脂质体生物等效性研究技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指
导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
附件:注射用两性霉素B脂质体生物等效性研究技术指导原则
国家药监局药审中心
2022年11月21日
为不断丰富完善仿制药个药指导原则并持续推进一致性评价工作,进一步指导氯雷他定片生物等效性研究的实施和评价,药审中心组织
起草了《氯雷他定片生物等效性研究技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》
(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年11月21日
为不断丰富完善仿制药个药指导原则并持续推进一致性评价工作,进一步指导富马酸丙酚替诺福韦片生物等效性研究的实施和评价,药
审中心组织起草了《富马酸丙酚替诺福韦片生物等效性研究技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原
则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
附件:富马酸丙酚替诺福韦片生物等效性研究技术指导原则
国家药监局药审中心
2022年11月21日
现阶段国内尚无抗肿瘤光动力治疗药物临床研发相关技术指导原则,现有的指导原则尚不能涵盖和专门针对抗肿瘤光动力治疗药物的临
床试验设计的考虑,为进一步明确技术原则,提高新药研发效率,化药临床一部相关适应症小组组织撰写了《抗肿瘤光动力治疗药物临床研
发技术指导原则》,形成征求意见稿,供药物研发相关人员参考。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:张虹、胡文娟
联系方式:zhanghong@cde.org.cn,huwj@cde.org.cn
感谢您的参与和大力支持。
药品审评中心
2022年11月25日
患者参与到药物研发的全生命周期中,符合以临床价值为导向的药物研发宗旨。为了便于申请人通过组织工作,更好地获得患者的体验
信息和数据,在国家药品监督管理局的部署下,药审中心组织制定了《组织患者参与药物研发的一般考虑指导原则(试行)》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同
意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年11月21日
一、培训时间
2022年11月23日11:10-12:00
二、培训方式
采用在线平台进行线上直播。
三、参加人员
面向全社会公开,药品生产企业注册、研发相关人员。
四、培训议程
此次培训不收取报名费,参训人员扫描二维码注册即可。
五、报名注册
电脑链接:
https://wx.vzan.com/live/pc/expo/index/1739?zbid=1772732231
六、联系方式
会议组织:张老师(010-882210382)
技术支持:郭老师(13810338321)
特应性皮炎是一种慢性、复发性、炎症性皮肤病,同时可合并其他疾病,大多初发于婴儿期,部分患者迁延到成年,严重影响生活质
量,目前尚无有效治疗手段。为规范该领域药物的研发与评价,我中心起草了《特应性皮炎治疗药物临床试验技术指导原则》,经中心内部
讨论,已形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人: 钱思源、葛玉梅
联系方式: qiansy@cde.org.cn、geym@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年11月18日
干眼是一种多因素引起的慢性眼表疾病,患病率高、严重影响患者视觉与生活质量、尚缺乏有效治疗手段。由于目前该病诊断和分类标
准尚不统一、多因素影响疾病特征和进程、疾病症状和体征分离、患者感受和疾病状态检测的内在变异性等,使干眼治疗药物的临床试验设
计和评价面临巨大挑战。为满足干眼治疗药物创新研发的需要,我中心起草了《干眼治疗药物临床试验技术指导原则》,经中心内部讨论,
已形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:翟云,赵聪
联系方式:zhaiy@cde.org.cn, zhaoc@cde.org.cn,
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年11月18日
多发性硬化是一种免疫介导的中枢神经系统慢性炎性脱髓鞘性疾病,临床表现、疾病分型、病理生理学过程复杂多样,使多发性硬化治
疗药物的临床试验设计和评价面临巨大挑战。为满足多发性硬化治疗药物创新研发的需要,我中心起草了《多发性硬化治疗药物临床试验设
计技术指导原则》,经中心内部讨论,已形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:翟云,唐崇淇
联系方式:zhaiy@cde.org.cn, tangchq@cde.org.cn,
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年11月18日
为规范审评过程中审评计时中止和恢复管理,保障药品审评过程合法合规、公平公正,在国家药品监督管理局的统一部署下,药审中心
制定了《国家药品监督管理局药品审评过程中审评计时中止与恢复管理规范(试行)》。经国家药品监督管理局审核同意,现予发布,自发
布之日起实施。
附件:国家药品监督管理局药品审评过程中审评计时中止与恢复管理规范(试行)
国家药监局药审中心
2022年11月15日
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个月。
您的反馈意见请发到以下联系人的邮箱:
联系人:王水强,王娜
联系方式:wangshq@cde.org.cn;wangn @cde.org.cn
感谢您的参与和大力支持。
药品审评中心
2022年11月16日
为了对双特异性抗体抗肿瘤药物临床研发中需要特殊关注的问题提出建议,指导企业更加科学地进行双特异性抗体临床研发,药审中心
在国家药品监督管理局的部署下,组织制定了《双特异性抗体抗肿瘤药物临床研发技术指导原则》(见附件)。根据《国家药监局综合司关
于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起
施行。
特此通告。
国家药监局药审中心
2022年11月9日
为配合《药品注册管理办法》的贯彻实施,进一步规范药品注册申请审评期间的变更,保证药品安全、有效和质量可控,药审中心组织
制定了《药品注册申请审评期间变更工作程序(试行)》(见附件),经国家药品监督管理局审查同意,现予以发布,自发布之日起实施。
国家药监局药审中心
2022年11月9日
为进一步规范和指导药物临床研发和评价中的获益-风险评估,提供可参考的技术规范,我中心起草了《新药获益-风险评估技术指导原
则》,经中心内部讨论,已形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:赵建中,何春俐
联系方式:zhaojzh@cde.org.cn;hechl@cde.org.cn
感谢您的参与和大力支持。
药品审评中心
2022年11月8日
为规范和指导已上市化学药品药学变更时的溶出曲线研究,提供可参考的技术标准,在国家药品监督管理局的部署下,药审中心组织制
定了《〈已上市化学药品药学变更研究技术指导原则(试行)〉溶出曲线研究的问答》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年11月7日
为了规范和指导化学仿制药口服调释制剂的药学研发,在国家药品监督管理局的部署下,药审中心组织制定了《化学仿制药口服调释制
剂乙醇剂量倾泻试验药学研究技术指导原则》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同
意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年11月7日
与成人抗肿瘤药物的研发热度相比,儿童抗肿瘤药的研发明显不足。儿童肿瘤治疗领域存在更为迫切的临床需求;同时,相较于成人,
儿童抗肿瘤药物研发的难度也更大。
为了对儿童抗肿瘤新药的临床研发提供思路和技术建议,药品审评中心组织撰写了《儿童抗肿瘤药物临床研发技术指导原则》,形成征
求意见稿,供药物研发的申请人和研究者参考。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:唐凌,宋媛媛
联系方式:tangl@cde.org.cn,songyy@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年11月8日
为进一步鼓励儿童用药研发生产,满足儿童用药需求,保障儿童用药安全,在国家药品监督管理局的部署下,药审中心组织制定了《儿
童用药口感设计与评价的技术指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药
监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年10月28日
根据国家局2019年3月28日发布的《关于发布化学仿制药参比制剂遴选与确定程序的公告》(2019年第25号),我中心组织遴选了第
六十三批参比制剂(见附件),现予以公示征求意见。
公示期间,请通过参比制剂遴选申请平台下“参比制剂存疑品种申请”模块向药审中心进行反馈,为更好服务申请人,反馈意见请提供
充分依据和论证材料,反馈材料应加盖单位公章,并提供真实姓名和联系方式。
公示期限:2022年10月29日~2022年11月11日(10个工作日)。
国家药品监督管理局药品审评中心
2022年10月28日
临床试验方案是药审中心对临床试验申请开展审评和基于临床试验方案进行沟通交流的核心资料,临床试验方案设计关系到药物临床试
验的质量,同时也是保障受试者安全和获得高品质数据的关键内容。为提高申请人撰写临床试验方案的质量、规范针对临床试验方案的沟通
交流和各类注册申请,提高临床试验方案的审评质量,加强对申请人的技术指导,我中心起草了《药物临床试验方案审评工作规范(征求意
见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:赵晨阳
联系方式:zhaochy@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年10月27日
近年来,人乳头瘤病毒(HPV)疫苗的研发如火如荼,多个HPV疫苗获批开展临床试验,型别从二价到十五价不等。HPV疫苗研发周期
长,研发成本高昂,为指导疫苗企业规范研发,加快相关产品的上市,我中心起草了《人乳头瘤病毒疫苗临床试验技术指导原则(征求意见
稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:刘亚琳,李英丽
联系方式: liuyalin@cde.org.cn,liyl@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年10月26日
新药临床安全性评价是新药获益-风险评估的重要基础。为进一步科学指导新药安全性评价,我中心起草了《新药临床安全性评价技术指导原则》,经中心内部讨论,已形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个月。
您的反馈意见请发到以下联系人的邮箱:
联系人:华尉利,林琳
联系方式:huawl @cde.org.cn;linl@ cde.org.cn
感谢您的参与和大力支持。
药品审评中心
2022年10月25日
为明确化学合成多肽药物的药学研究技术要求,以更好的指导企业进行研究以及统一监管要求,我中心经调研以及与专家和业界讨论,
组织起草了《化学合成多肽药物药学研究技术指导原则(征求意见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
请将您的反馈意见发到以下联系人的邮箱。
联系人:何驰宇;姜喜凤;胡玉玺
邮箱:hechy@cde.org.cn ;jiangxf@cde.org.cn; huyuxi@cde.org.cn
感谢您的参与和大力支持。
药品审评中心
2022年10月25日
为进一步规范和指导慢性乙型肝炎治疗药物临床试验,提供可参考的技术规范,我中心起草了《慢性乙型肝炎治疗药物临床试验技术指
导原则》,经中心内部讨论,已形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:左书凝,何春俐
联系方式: zuoshn@cde.org.cn; hechl@cde.org.cn
感谢您的参与和大力支持。
药品审评中心
2022年10月25日
为进一步加强质量风险管理在产品质量控制中的应用,提高非无菌化学药品及原辅料微生物限度标准制定的科学性及合理性,明确申报
资料中微生物限度研究及控制的相关要求,我中心经调研以及与专家和业界讨论,组织起草了《非无菌化学药品及原辅料微生物限度研究技
术指导原则(征求意见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
请将您的反馈意见发到以下联系人的邮箱。
联系人:李珊珊;赵磊;王伟萍
邮箱:lishsh@cde.org.cn;zhaolei@cde.org.cn;wangwp@cde.org.cn
感谢您的参与和大力支持
药品审评中心
2022年10月10日
近年来,基因治疗已成为研发热点之一,该类产品具有创新性和复杂性,有必要对临床试验设计提出要求和提供指导。我中心在充分调
研的基础上起草了《基因治疗血友病临床试验设计技术指导原则(征求意见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人: 黄云虹,赵晨阳
联系方式: huangyh@cde.org.cn,zhaochy@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年10月9日
根据国家局2019年3月28日发布的《关于发布化学仿制药参比制剂遴选与确定程序的公告》(2019年第25号),我中心组织遴选了第
六十三批参比制剂(见附件),现予以公示征求意见。
公示期间,请通过参比制剂遴选申请平台下“参比制剂存疑品种申请”模块向药审中心进行反馈,为更好服务申请人,反馈意见请提供
充分依据和论证材料,反馈材料应加盖单位公章,并提供真实姓名和联系方式。
公示期限:2022年10月9日~2022年10月20日(10个工作日)。
国家药品监督管理局药品审评中心
2022年10月9日
肿瘤治疗性疫苗作用机制是通过抗原呈递细胞(APC)将抗原加工并呈递给T细胞,从而诱导产生或放大已存在的抗原特异性T细胞反
应,这一系列的免疫反应过程需要较长时间。与传统细胞毒药物、靶向治疗或其它肿瘤免疫治疗药物相比,肿瘤治疗性疫苗的临床试验设计
存在诸多不同考虑。考虑到国内尚无相关指导原则对这类产品的临床设计进行规范指导,我中心在充分调研国内外同品种研发情况以及相关
临床试验技术要求基础上,起草了《肿瘤治疗性疫苗临床试验技术指导原则(征求意见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:刘妍彤,高建超
联系方式:liuyt@cde.org.cn, gaojch@cde.org.cn。
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年10月9日
为不断丰富完善仿制药个药指导原则并持续推进一致性评价工作,进一步指导阿司匹林肠溶片生物等效性研究的实施和评价,药审中心
组织起草了《阿司匹林肠溶片生物等效性研究技术指导原则》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。
特此通告。
附件:阿司匹林肠溶片生物等效性研究技术指导原则
国家药监局药审中心
2022年9月30日
为进一步指导评估药物临床试验中药物性肝损伤的潜在可能性,保障受试者安全,同时获得安全性信息以评估试验药物的风险特征。我
中心起草了《临床试验中药物性肝损伤的识别、处理及评价指导原则》,经中心内部讨论,已形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:陈颖,何春俐
联系方式:cheny@cde.org.cn;hechl@ cde.org.cn
感谢您的参与和大力支持。
药品审评中心
2022年10月8日
近年来,随着大量免疫相关治疗药物研发申报涌现,药物对免疫系统的安全性已成为一个备受瞩目的问题。现有ICH S8指导原则主要针
对化学药物,不包含生物制品。国内目前尚无较为全面的针对化药和生物制品免疫毒性的指导原则。为更好地引导药物研发过程中对潜在免
疫毒性的评价,药品审评中心组织撰写了《药物免疫毒性非临床研究技术指导原则》。经中心内部讨论,并征求部分学术界和工业界专家意
见,现形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:闫莉萍、刘轶博
联系方式:yanlp@cde.org.cn,liuyb@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年9月30日
根据财政部关于稳步推广电子非税收入一般缴款书工作要求,国家药监局决定启用药品、医疗器械产品注册费电子缴款书。现将有关事
项通告如下:
一、申请人在国家药品监督管理局网上办事大厅提交药品、医疗器械产品注册申请,相关审评中心将进行审核,确认无误后财政部非税
收入收缴管理系统将以短信形式向申请人发送电子缴款码,申请人可通过柜台缴款、自助终端、网上缴款、自助POS刷卡、银行汇兑、划缴
缴款等方式进行缴款。国家药品监督管理局行政事项受理服务和投诉举报中心确认应缴费用到账后,将于10个工作日内将电子缴款书发送至
申请人指定的电子邮箱。
二、电子缴款书与纸质票据具有同等法律效力。
三、电子缴款书自本通告发布之日起正式启用。
特此通告。
国家药监局
2022年8月22日
药物临床依赖性研究是具有潜在滥用风险的新药上市前的重要研究内容,我国尚无专门技术要求对此类研究进行规范管理。在国家药品
监督管理局的部署下,药审中心组织制定了《药物临床依赖性研究技术指导原则(试行)》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。
特此通告。
附件:药物临床依赖性研究技术指导原则(试行)
国家药监局药审中心
2022年9月26日
为加快建立和完善符合中药特点的技术评价体系,促进基于人用经验的中药复方制剂新药的研发注册,药审中心起草了《基于人用经验
的中药复方制剂新药药学研究技术指导原则》。经征求中心内部各相关专业以及专家、研发单位意见,形成征求意见稿。现在中心网站予以
公示,以广泛听取各界意见和建议。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起一个
月。
您的反馈意见请发到邮箱:zyyxzdyz@cde.org.cn (邮箱名为“中药药学指导原则”拼音首字母)
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年9月27日
为加快建立和完善符合中药特点的技术评价体系,促进基于我国中药新药研发创新,药审中心起草了《中药新药临床试验用药品的制备
研究技术指导原则》。经征求中心内部各相关专业以及专家、研发单位意见,形成征求意见稿。现在中心网站予以公示,以广泛听取各界意
见和建议。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起一个
月。
您的反馈意见请发到邮箱:zyyxzdyz@cde.org.cn (邮箱名为“中药药学指导原则”拼音首字母)
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年9月27日
现阶段国内尚无治疗卵巢癌新药临床研发相关技术指导原则,现有的指导原则尚不能涵盖和专门针对卵巢癌的临床试验设计的考虑,为
进一步明确技术原则,提高新药研发效率,化药临床一部相关适应症小组组织撰写了《治疗卵巢癌新药临床研发技术指导原则》,形成征求
意见稿,供药物研发相关人员参考。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:张虹、胡文娟
联系方式:zhanghong@cde.org.cn,huwj@cde.org.cn
感谢您的参与和大力支持。
药品审评中心
2022年9月26日
为明确对咀嚼片(化学药品)质量属性研究的技术要求,以更好地指导企业进行研究以及统一监管要求,我中心经调研以及与专家和业
界讨论,组织起草了《咀嚼片(化学药品)质量属性研究技术指导原则(征求意见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
请将您的反馈意见发到以下联系人的邮箱。
联系人:吴小飞;王宏亮
邮箱:wuxf@cde.org.cn;wanghl@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年9月26日
近年来,国内外细胞和基因治疗产业进展迅速,新技术、新应用、新成果不断涌现,在恶性肿瘤、再生医学等多种疾病领域显示出巨大的
应用潜力。为加快推动我国生物医药产业发展,建立更加科学完善的技术评价体系,加强与临床机构、研发企业的沟通交流,药审中心拟定
于2022年9月28日举办“细胞和基因治疗产品药学研究与评价审评考虑”线上培训宣讲会。现将有关事项通知如下:
一、会议时间
2022年9月28日14:00-16:30
二、会议方式
采用在线平台进行线上直播。
三、参加人员
面向全社会公开,创新药物研发相关临床机构、制药企业人员。
四、主要内容
介绍《体内基因治疗产品药学研究与评价技术指导原则(试行)》《免疫细胞治疗产品药学研究与评价技术指导原则(试行)》《体外
基因修饰系统药学研究与评价技术指导原则(试行)》,具体议程见附件。
五、报名注册
1. 此次培训不收取报名费,参会人员需要扫描二维码进入注册即可。名额有限,报完为止。
或者输入网址打开报名页面建议使用谷歌或者360浏览器
(确保网络稳定)
https://wx.vzan.com/live/pc/expo/index/1562?zbid=1772732231
2. 请参与培训的学员,注册后通过问题收集页面,提交需要讲者回复的问题,讲者授课后进行答疑与研讨。
附:“细胞和基因治疗产品药学研究与评价审评考虑”指导原则宣讲会议程
国家药品监督管理局药品审评中心
2022年9月23日
9月14日,由国家药品监督管理局药品审评中心(以下简称药审中心)指导、中国药品监督管理研究会主办的《创新药及罕见病药物研
发技术指导原则培训会》在线直播培训顺利召开,中国药品监督管理研究会时立强副会长兼秘书长致辞。
此次培训会授课邀请到药审中心化药药学一部主审审评员张耀老师、化药临床二部审评员徐小文老师、化药药学一部主审审评员刘永辉
老师、化药临床一部审评员赵伯媛老师围绕《境外已上市境内未上市化学药品药学研究与评价技术要求(试行)》、《境外已上市境内未上
市药品临床技术要求》、《化学药品创新药上市申请前会议药学共性问题及相关技术要求》、《罕见疾病药物临床研发技术指导原则》进行
了详细的解读与答疑。来自446余家制药企业和临床机构、456位监管机构人员共计902人报名观看了本场培训会。
为促进和指导儿科药物研发,我中心组织起草了《成人用药数据外推至儿科人群的定量方法学指导原则(征求意见稿)》,现公开征求
意见。欢迎各界提出宝贵意见和建议,并请及时反馈给我们。
征求意见时限为自发布之日起1个月。
请将您的反馈意见发到邮箱:衡明莉 hengml@cde.org.cn 高丽丽 gaolili@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年9月19日
生物制药技术的发展,推动抗体偶联药物进入高速发展阶段,尤其是在肿瘤治疗领域,抗体偶联抗肿瘤药物的研发持续增长。
为了对抗体偶联抗肿瘤药物的临床研发中需要特殊关注的问题提出建议,并指导企业开展更为科学的临床研发,药品审评中心组织撰写
了《抗肿瘤抗体偶联药物临床研发技术指导原则》,形成征求意见稿,供药物研发相关人员参考。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:夏琳,宋媛媛
联系方式:xialin@cde.org.cn,songyy@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年9月15日
为进一步指导我国创新药物研发,加快罕见病药品研发上市进程,加强与临床机构、研发企业的沟通交流,提升我国创新药研发水平和
效率,药审中心定于2022年9月21日举办“创新药物临床研发在不同适应症领域的审评考虑”线上培训。现将有关事项通知如下:
一、会议时间
2022年9月21日14:00-17:30
二、会议方式
采用在线平台进行线上直播。
三、参加人员
面向全社会公开,创新药物研发相关临床机构、制药企业人员。
四、主要内容
介绍创新药物临床研发在不同适应症领域的审评考虑,具体议程见附件。
五、报名注册
1. 此次培训不收取报名费,参会人员需要扫描二维码进入注册即可。名额有限,报完为止。
2. 请参与培训的学员,注册后通过问题收集页面,提交需要讲者回复的问题,讲者授课后进行答疑与研讨。
附:“创新药物临床研发在不同适应症领域的审评考虑”指导原则宣讲会议程
为了鼓励创新和制药现代化,助力ICH Q13指导原则在国内的落地实施,同时也为了指导企业研发,统一审评尺度,我中心组织起草了
《化药口服固体制剂连续制造技术指导原则(征求意见稿)》,现向社会各界征求意见。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。
征求意见时限为自发布之日起1个月。
您的反馈意见请发到以下联系人的邮箱:
联系人:胡延臣,冯雪
联系方式:huych@cde.org.cn,fengx@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年9月9日
为推动新修订的ICH指导原则在国内的平稳落地实施,我中心拟定了《Q3D(R2):元素杂质指导原则》实施建议,同时组织翻译中
文版。现对Q3D(R2)实施建议和中文版公开征求意见,为期1个月。
如有修改意见,请反馈至联系人电子邮箱:gkzhqyj@cde.org.cn。
附件:1.Q3D(R2)实施建议
2.Q3D(R2)中文版
3.Q3D(R2)英文版
国家药品监督管理局药品审评中心
2022年9月8日
复方药物是指含有两种或两种以上已知活性成份的药物。复方药物是改良型新药的一种重要类型,其临床研发具有特殊性。复方药物临
床试验的设计取决于复方的立题和治疗目标。复方药物的研发涉及不同适应症领域、不同疾病和活性成分的特性,但其临床研发具有共性的
技术考虑。
为了科学引导企业合理地开发复方药物,进一步明确临床试验技术标准,我中心起草了《复方药物临床试验技术指导原则(征求意见
稿)》,经中心内部讨论,已形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:华尉利,徐小文
联系方式:xuxw@cde.org.cn, huawl@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年9月7日
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。
征求意见时限为自发布之日起1个月。
您的反馈意见请发到以下联系人的邮箱:
联系人:张芸,李越,张慧,张钊瑞
联系方式:liy@cde.org.cn,zhanghui@cde.org.cn,zhangzhr@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年9月5日
根据国家局2019年3月28日发布的《关于发布化学仿制药参比制剂遴选与确定程序的公告》(2019年第25号),我中心组织遴选了第
六十二批参比制剂(见附件),现予以公示征求意见。
公示期间,请通过参比制剂遴选申请平台下“参比制剂存疑品种申请”模块向药审中心进行反馈,为更好服务申请人,反馈意见请提供
充分依据和论证材料,反馈材料应加盖单位公章,并提供真实姓名和联系方式。
公示期限:2022年8月30日~2022年9月13日(10个工作日)。
国家药品监督管理局药品审评中心
2022年8月30日
为加强药品说明书及标签的规范管理,指导临床正确使用药品,促进企业有序开展起草和完善说明书及标签中药学信息的相关工作,我
中心组织制订了《化学药品说明书及标签药学相关信息撰写指导原则(征求意见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起一个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:刘涓、陈淼
联系方式:liuj@cde.org.cn、chenm@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年8月30日
为明确溶液型滴眼剂仿制药的药学研究技术要求,以更好的指导企业进行研究以及统一监管要求,我中心经调研以及与专家和业界讨
论,组织起草了《溶液型滴眼剂仿制药药学研究技术指导原则(征求意见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
请将您的反馈意见发到以下联系人的邮箱。
联系人:田娜;魏婷婷
邮箱:tiann@cde.org.cn;weitt@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年8月29日
经国家药品监督管理局仿制药质量和疗效一致性评价专家委员会审核确定,现发布仿制药参比制剂目录(第五十七批)。
特此通告。
附件:仿制药参比制剂目录(第五十七批)
国家药监局
2022年8月25日
为进一步推动提升国内审评人员和工业界对ICH《Q13:连续制造》指导原则相关技术要求的理解与掌握,加强与国际监管机构和工业
界专家关于审评和企业注册申报实践中应用连续制造的交流,药审中心与中国药品监督管理研究会定于2022年8月26日共同举办《连续制造
相关概念及实例研究》线上培训。现将培训有关事项通知如下:
一、培训时间
时间:2022年8月26日上午9:00-17:10
二、组织机构
主办单位:国家药品监督管理局药审中心
承办单位:中国药品监督管理研究会
三、参加人员
面向全社会公开,线上名额共计10000人。
四、主要内容及授课专家
此次培训将邀请来自国外监管机构的ICH Q13专家工作组(EWG)专家和具有连续制造实践经验的企业专家担任讲者,进行连续制造
技术要求解读和案例分享(培训方案见附)。
五、报名注册
1.此次培训不收取报名费,参会人员需要扫描二维码进入注册即可。名额有限,报完为止。
2.请参与培训的学员,注册后通过问题收集页面,提交需要对应专家回复的问题,专家授课后进行答疑与研讨。
六、联系方式
会议组织:张老师(010-82210382)
技术支持:郭老师(13810338321)
附:《连续制造相关概念及实例研究》培训日程
呼吸道合胞病毒是世界范围内引起5岁以下儿童急性下呼吸道感染最常见的病毒病原,是造成婴幼儿病毒性呼吸道感染住院的首要因
素。国内多家制药企业已开始呼吸道合胞病毒感染药物的研发。目前国内外尚参考的指导原则,为进一步明确技术标准,提高企业研发效
率。我中心起草了《呼吸道合胞病毒感染药物临床试验技术指导原则》,经中心内部讨论,已形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人: 赵建中、葛玉梅
联系方式: zhaojzh@cde.org.cn、geym@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年8月18日
为促进真实世界证据在药品注册申请中的应用实践,提高研发效率,针对申请人与审评机构开展真实世界证据支持注册申请的沟通交流
给出具体要求和指导性建议,我中心组织起草了《真实世界证据支持药物注册申请的沟通交流指导原则(征求意见稿)》,现公开征求意
见。欢迎各界提出宝贵意见和建议,并请及时反馈给我们。
征求意见时限为自发布之日起1个月。
请将您的反馈意见发到邮箱:赵骏 zhaojun@cde.org.cn 辛晓娜 xinxn@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年8月17日
为推动ICH三级指导原则在国内的平稳落地实施,我中心拟定了《M10:生物分析方法验证及样品分析》实施建议,同时组织翻译中文
版。现对M10实施建议和中文版公开征求意见,为期1个月。
如有修改意见,请反馈至联系人电子邮箱:gkzhqyj@cde.org.cn。
附件:1.M10指导原则实施建议
2.M10指导原则中文版
3.M10指导原则英文版
国家药品监督管理局药品审评中心
2022年8月17日
生理药代动力学模型目前在儿科人群药物研发方面应用广泛,为了合理规范使用该模型,药品审评中心组织起草了《生理药代动力学模
型在儿科人群药物研发中应用的技术指导原则(征求意见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,以便后续完善。征求意见时限为自发布之日起1个月。
请将您的反馈意见发到以下联系人的邮箱。
联系人:韩鸿璨、潘鹏玉、车津晶
联系方式:panpy@cde.org.cn;chejj@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年8月17日
为推动药品注册技术标准与国际接轨,经研究,国家药品监督管理局决定适用《E8(R1):临床研究的一般考虑》和《E14:非抗心律失常药物
致QT/QTc间期延长及潜在致心律失常作用的临床评价》国际人用药品注册技术协调会(ICH)指导原则。现就有关事项公告如下:
一、 自2023年7月31日起,启动的药物临床研究的相关要求适用《E8(R1):临床研究的一般考虑》和《E14:非抗心律失常药物致QT/QTc
间期延长及潜在致心律失常作用的临床评价》。E8(R1)实施之日起,E8停止实施。
二、相关技术指导原则可在国家药品监督管理局药品审评中心网站查询。国家药品监督管理局药品审评中心负责做好本公告实施过程中的相关技
术指导工作。
2022年8月1日
“以患者为中心”的药物研发是指以患者需求为出发点、视患者为主动参与者、以临床价值为最终目的,该理念已成为当前药物研发的
核心指导思想。为了指导以患者为中心的临床试验的设计,即不断了解患者需求,在符合科学性的原则下将有意义的患者体验数据纳入临床
试验设计要素的考量中,并充分关注受试者的感受,我中心起草了《以患者为中心的临床试验设计技术指导原则(征求意见稿)》,旨在阐
明以患者为中心的临床试验的一般原则、整体研发计划、以患者为中心的临床试验设计要素和其他考量,为临床试验设计提供指引和参考
。经中心内部讨论,已形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:陈颖,唐崇淇
联系方式:cheny@cde.org.cn,tangchq@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年8月9日
“以患者为中心”的药物研发理念已成为当前药物研发的核心指导思想。为了指导以患者为中心的临床试验的获益风险评估,将患者需
求纳入到药物的获益-风险评估体系中,我中心起草了《以患者为中心的临床试验获益-风险评估技术指导原则》,经征求专家意见及中心内
部讨论,已形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:杨靖怡,徐小文,王水强
联系方式:yangjy@cde.org.cn, xuxw@cde.org.cn, wangshq@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年8月9日
为鼓励创新,提高申请人和监管机构沟通交流的质量与效率,加快新药研发,我中心组织制订了《化学药品创新药Ⅲ期临床试验前会议
药学共性问题及相关技术要求(征求意见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起一个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:徐立华、赵蕾、赵一飞
联系方式:xulh@cde.org.cn、zhaol@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年08月02日
为进一步规范和指导原发性胆汁性胆管炎治疗药物临床试验,提供可参考的技术规范,我中心起草了《原发性胆汁性胆管炎治疗药物临
床试验技术指导原则》,经中心内部讨论,已形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:陈颖,林琳
联系方式:cheny@cde.org.cn;linl@ cde.org.cn
感谢您的参与和大力支持。
药品审评中心
2022年8月1日
“以患者为中心”的药物研发是指以患者需求为出发点、视患者为主动参与者、以临床价值为最终目的,该理念已成为当前药物研发的核心指导思想。为了实施更加患者可及、友好、便利的临床试验,药品审评中心组织起草了《以患者为中心的临床试验实施技术指导原则》的征求意见稿。
我们诚挚欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个月。
您可将意见发到中心联系人的邮箱。
联系人:钱思源 赵聪
邮箱:qiansy@cde.org.cn,zhaoc@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年8月9日
根据国家局2019年3月28日发布的《关于发布化学仿制药参比制剂遴选与确定程序的公告》(2019年第25号),我中心组织遴选了第
六十一批参比制剂(见附件),现予以公示征求意见。
公示期间,请通过参比制剂遴选申请平台下“参比制剂存疑品种申请”模块向药审中心进行反馈,为更好服务申请人,反馈意见请提供
充分依据和论证材料,反馈材料应加盖单位公章,并提供真实姓名和联系方式。
公示期限:2022年7月27日~2022年8月9日(10个工作日)。
国家药品监督管理局药品审评中心
2022年7月27日
予以公示,以广泛听取各界意见和建议。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:曾新
联系方式:zengxin@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年7月25日
某些用于治疗或预防由化学、生物、放射、核物质引起的严重威胁人体生命健康的疾病的药物因开展人体有效性试验不符合伦理或现场
试验不可行,无法按常规思路开展临床有效性试验获得人体有效性数据申报上市,需基于“动物法则(Animal Rule)”进行药物注册。为
了科学开展该类药物的有效性评价和正确应用动物法则,推动该类药物上市,我中心组织起草了《基于动物法则的药物注册技术指导原
则》,现在中心网站予以公示。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,以便后续完善。征求意见时限为自发布之日起1个月。
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年7月22日






为进一步促进药物临床试验期间安全性数据快速报告标准统一,提升数据质量,药审中心组织起草了《药物临床试验期间安全性数据快
速报告常见问答(2.0版)》,现在中心网站予以公示,广泛听取社会各界意见和建议。欢迎社会各界提出宝贵意见和建议,并请通过以下
邮箱及时反馈我中心。
征求意见时限:自公示之日起两周。
联系人:刘敏
征求意见邮箱:lium02@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年7月19日
为加强药品审评过程中风险控制,规范药品审评过程中有因检查启动工作,按照新版《药品注册管理办法》第四十九条规定,结合《药
品注册核查检验启动工作程序(试行)》《药品注册核查工作程序(试行)》和《药物警戒检查指导原则》相关程序要求。我中心组织起草
了《药品审评过程中有因检查启动工作程序(征求意见稿)》,现在中心网站予以公示。
欢迎社会各界提出宝贵意见和建议,以便后续完善。征求意见时限为自发布之日起1个月。
联系人:何辉;班浩
联系方式:oc_cde@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年7月7日
随着《药物警戒质量管理规范》的发布和实施,申办者应建立完善的药物警戒体系,对临床试验期间的安全风险管理承担主体责任,以
充分保护受试者安全。为更好的推动和指导申办者对临床试验期间的安全性信息及时评价和报告,明确技术标准和向监管机构报告的要求,
我们遵照国内法律法规要求,同时借鉴国际相关技术指南制定本指导原则。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起一个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:陈艳,赵婷婷
联系方式:chenyan@cde.org.cn,zhaott@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年7月13日
注射用两性霉素B脂质体,为特殊注射剂,生物等效性评价存在一定难度。我国尚无本品的生物等效性研究技术指导原则,为进一步规
范注射用两性霉素B脂质体的生物等效性研究,经广泛调研和讨论,我中心组织起草了《注射用两性霉素B脂质体生物等效性研究技术指导原
则(征求意见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,以便后续完善。征求意见时限为自发布之日起1个月。
请将您的反馈意见发到以下联系人的邮箱。
联系人:贺锐锐、刘美霞
邮 箱:herr@cde.org.cn、liumx@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年7月7日
征求意见时限为自发布之日起2个月。
请将您的反馈意见发到邮箱:赵骏 zhaojun@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年7月7日
为进一步明确化学仿制药口服调释制剂乙醇剂量倾泻试验具体试验方法设计,以更好的指导企业进行研究以及统一监管要求,我中心经
调研以及与专家和业界讨论,组织起草了《化学仿制药口服调释制剂乙醇剂量倾泻试验药学研究技术指导原则(征求意见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
请将您的反馈意见发到以下联系人的邮箱。
联系人:司晓菲;姜典卓
邮箱:sixf@cde.org.cn;jiangdzh@cde.org.cn
感谢您的参与和大力支持。
药品审评中心
2022年7月7日
抗体偶联药物(antibody-drug conjugate,ADC)通常由抗体和小分子化合物偶联而成,通过抗体的特异性和靶向性,靶向运送小分
子化合物至作用部位,不仅可提高药物治疗效果,还可降低小分子化合物对非靶组织、非靶细胞的毒性。近年,ADC已在恶性肿瘤等疾病领
域显示出巨大的应用潜力,全球已批准14个ADC药物上市,国内ADC药物发展也较为迅速,已有1个本土创新ADC药物获批上市,并有数十
个ADC药物获批开展临床研究。目前ADC药物的研发一般参考ICH S9、ICH S6等相关指导原则,国内外尚无ADC药物的针对性指导原则。
为更好指导和促进ADC药物的研究和开发,我中心组织起草了《抗体偶联药物非临床研究技术指导原则》,经中心内部讨论,并征求部分学
术界和工业界专家意见,现形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起一个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:闫莉萍、周围
联系方式:yanlp@cde.org.cn,zhouw@cde.org.cn
国家药品监督管理局药品审评中心
2022年7月6日
申办者基于何种原则、如何开展组织患者参与到药物研发工作中,从而获得患者体验信息和数据,是药物研发的关键要素。我国尚无此
类指导原则出台,为便于申办者开展相关组织工作,我中心起草了《组织患者参与药物研发的一般考虑指导原则》,经中心内部讨论,已形
成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:王洪航、王晶
联系方式:85243050、85243063
wanghh@cde.org.cn、wangjing01@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年7月6日
根据国家局2019年3月28日发布的《关于发布化学仿制药参比制剂遴选与确定程序的公告》(2019年第25号),我中心组织遴选了第
六十批参比制剂(见附件),现予以公示征求意见。
公示期间,请通过参比制剂遴选申请平台下“参比制剂存疑品种申请”模块向药审中心进行反馈,为更好服务申请人,反馈意见请提供
充分依据和论证材料,反馈材料应加盖单位公章,并提供真实姓名和联系方式。
公示期限:2022年7月5日~2022年7月18日(10个工作日)。
国家药品监督管理局药品审评中心
2022年7月5日
经国家药品监督管理局仿制药质量和疗效一致性评价专家委员会审核确定,现发布仿制药参比制剂目录(第五十五批)。
特此通告。
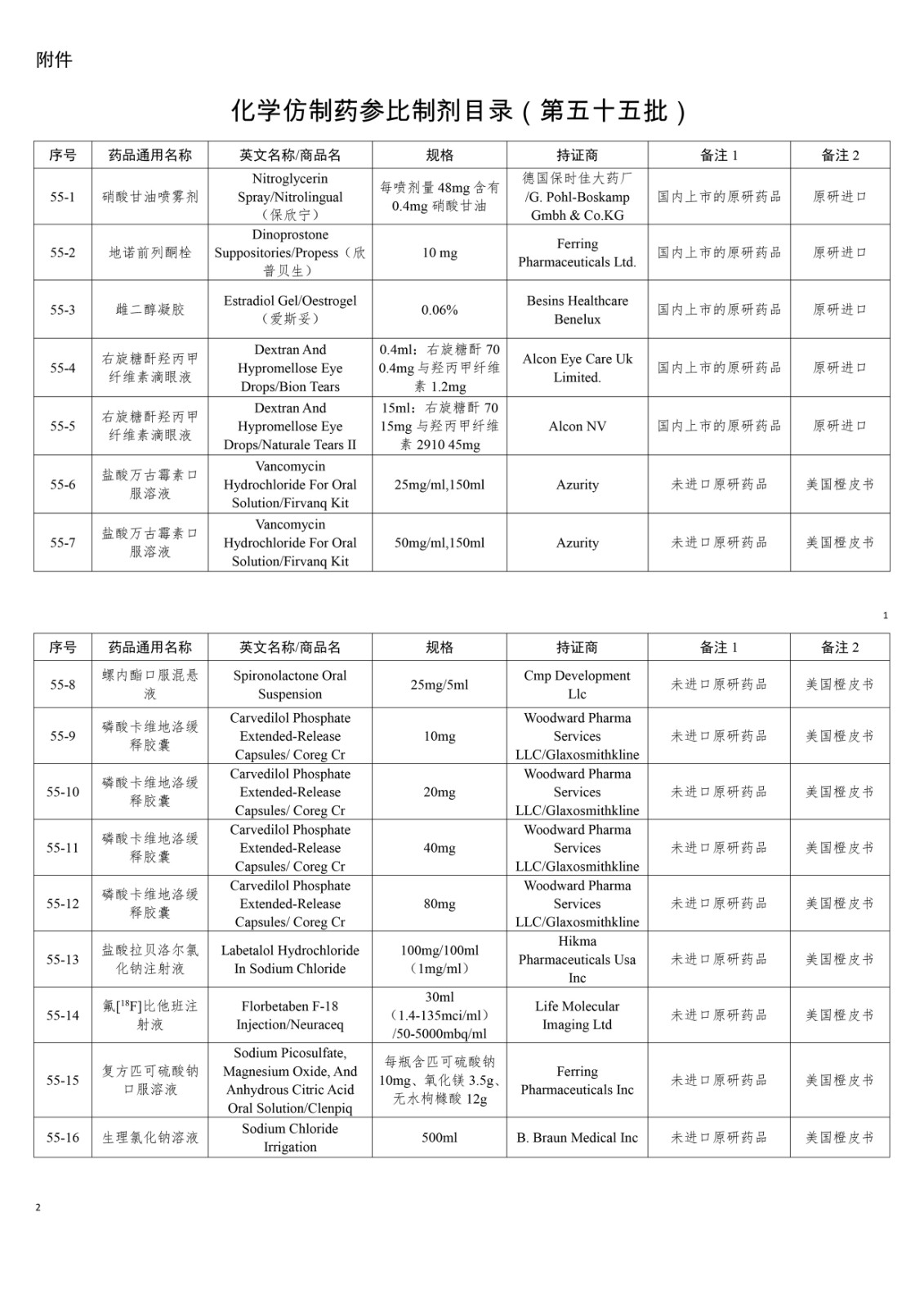
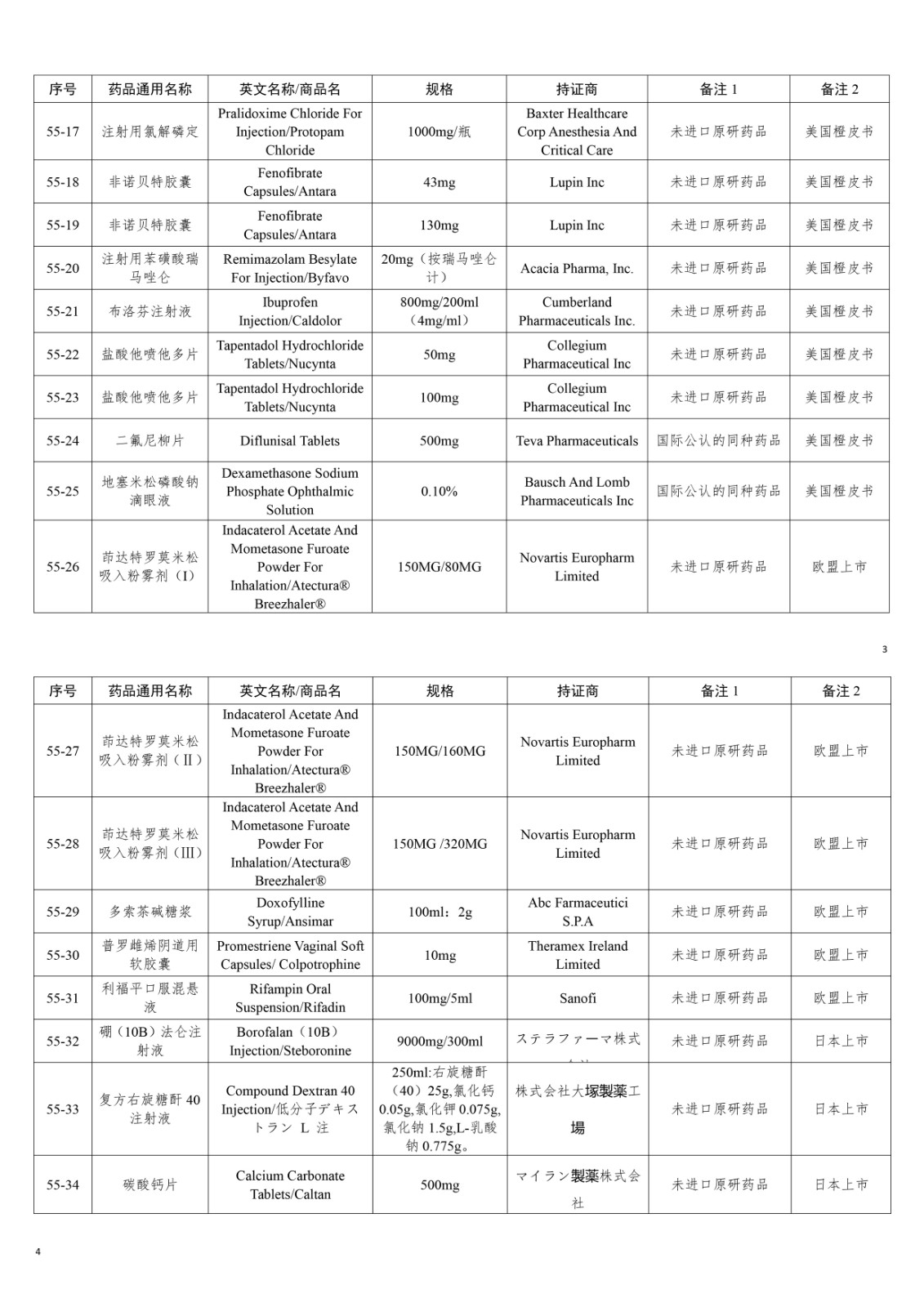
国家药品监督管理局食品药品审核查验中心(国家疫苗检查中心)(以下简称“核查中心”)是国家药品监督管理局(以下简称“国家
药监局”)所属事业单位,承担药物临床试验、非临床研究机构资格认定(认证)和研制现场检查,药品注册核查,药品生产环节的有因检
查、药品境外检查,以及疫苗巡查和血液制品抽查等相关工作。
2021年,核查中心以习近平新时代中国特色社会主义思想为指导,深入贯彻落实习近平总书记重要指示批示精神,坚持以人民为中心,
以“四个最严”为根本遵循,担当作为、攻坚克难,持续加强药品检查核查工作。在国家药监局的统一领导下,以疫情为命令,冲锋在新
冠病毒疫苗、新冠病毒治疗药物检查工作的第一线,统筹开展疫情防控和检查核查工作,积极探索远程检查工作,有效推进检查机构质量
体系和能力建设,整合资源加大信息公开力度,积极参与国际交流,持续加强职业化专业化检查员队伍建设,努力提高检查核查工作质量
和效率。
一、做好各项检查工作,维护公众用药安全
2021年,核查中心共组织完成药品检查核查任务1368个。其中,药品注册核查任务1214个,占比约88.7%;药品监督检查任务101个,
占比约7.4%;药品境外检查任务6个,占比约0.4%;许可检查任务47个,占比约3.4%。
(一)药品注册核查
药品注册核查是药品审评审批的重要环节,通过对申报资料的真实性、一致性以及药品上市商业化生产条件进行核实,检查申请人研制
过程的合规性、数据可靠性等。2021年,核查中心完成药品注册核查任务1214个,包括临床试验及上市许可申请等注册核查任务1066个、
仿制药质量和疗效一致性评价核查任务148个,保障了药品审评审批工作的顺利开展,支持了药品生产企业复工复产。2021年,药品注册核
查不通过的任务共10个。
药理毒理学研究核查中发现的主要问题包括:部分实验动物的检测数据不一致;数据重测和结果取舍无相关标准操作规程;数据处理执
行标准不一致;仪器使用和维护记录、受试物接收及运输记录不完整等。药物临床试验数据核查中发现的主要问题包括:原始病历记录不
详细、不完整;方案偏离未报告;个别量表的填写和修改不规范;试验用药的记录不准确;安全性信息记录不完整;合并用药记录不全等。
药学研制和生产现场核查中发现的主要问题包括:部分数据存在无法溯源、记录不完整等数据可靠性问题;部分原始记录与申报资料不一致
;技术转移不充分;确认与验证不充分;不具备商业化生产条件等。
(二)药品监督检查
药品监督检查是对药品上市许可持有人、药品生产企业执行有关法律、法规,实施药品生产质量管理规范等方面开展的检查工作,核查
中心按照国家药监局的工作部署,开展基于风险的监督检查。2021年,核查中心完成监督检查任务101个,包括中药监督检查任务10个、
化学药品监督检查任务5个、疫苗巡查、血液制品抽查及其他生物制品检查任务84个、麻醉精神类药品安全管理检查任务2个,对促进药品
上市许可持有人和生产企业持续合规发挥了积极作用。2021年,药品监督检查不通过的任务共3个。
药品监督检查发现的主要问题包括:质量受权人未按程序要求履行物料和产品放行职责;实际生产批量超出工艺验证批量范围;企业无
法提供检验结果偏差的调查记录;企业厂房维护、设备清洁及生产过程粉尘控制措施不足,存在污染和交叉污染的风险等。
(三)境外检查
境外检查是对生产地在境外的药品生产企业开展的现场检查。新冠肺炎疫情发生后,由于出入境的限制,核查中心努力探索境外远程非
现场的检查模式。2021年,核查中心采取境外远程非现场方式完成检查任务6个,有力保障了进口药品质量安全。2021年,境外远程非现
场检查不通过的任务1个。
药品境外检查发现的主要问题包括:在药品生产用原料、辅料和成品的质量控制方面存在严重不足;对反复、多次出现可见异物投诉情
况采取的纠正与预防措施不足;未对变更进行有效控制;未对关键的生产工艺和操作规程定期进行再验证;质量协议中关于原料药放行职
责约定不明确等。
(四)许可检查
许可检查是药品监督管理部门在开展药品生产经营许可申请审查过程中,对申请人是否具备从事药品生产经营活动条件开展的检查。
2021年,核查中心共开展许可检查任务47个,包括放射性药品许可检查任务9个和药物非临床研究质量管理规范(GLP)认证检查任务38
个。2021年,GLP认证检查不通过的任务共1个。
GLP认证检查发现的主要问题包括:质量保证部门履职能力不足;机构负责人资质不符合要求;实验动物设施设计与管理不到位;试验
环节未能严格执行操作规程;计算机账户权限分级设置不合理等。
放射性药品许可检查发现的主要问题包括:文件制定不规范;验证内容不完善;未严格执行供应商审计规定等。
二、积极推进制度建设,规范检查核查工作
(一)发布《药品注册核查工作程序(试行)》及其配套文件
《药品注册管理办法》(2020年修订)调整了药品注册审评审批工作流程,重新确定了注册核查工作责任主体,明确了注册核查的工作
内容和目的。为更好地服务注册申请人,加强药品注册核查管理,规范药品注册核查工作程序,2021年,核查中心组织起草并发布了5个
配套文件,包括《药品注册核查工作程序(试行)》、3个核查要点与判定原则,以及《药品注册生产现场核查和上市前药品生产质量管理
规范检查衔接工作程序(试行)》(以下简称《衔接程序》),并于2022年1月1日起正式施行。其中,《衔接程序》为核查中心负责开展
的药品注册生产现场核查和省级药品监管部门负责开展的上市前药品生产质量管理规范(GMP)检查建立了衔接工作程序,以保证药品注
册核查与上市前药品GMP检查的有机衔接。
(二)《药品生产质量管理规范-细胞治疗产品附录》征求意见
2021年,为加强对细胞治疗产品的监管,结合细胞治疗产品在生产管理过程中的实际情况,提升法规的可执行性,核查中心组织对
《GMP-细胞治疗产品附录》进行完善和细化。国家药监局已发布新版征求意见稿,再次面向社会公开征求意见。
(三)修订药品检查工作规范和技术指南
2021年,核查中心对药品检查的工作规范和技术指南进行起草和修订,组织起草《临床试验用药品生产质量管理规范》《药包材生产质
量管理规范》,组织编写《药品共线生产质量管理指南》《吸入制剂现场检查指南(征求意见稿)》,参与国际人用药品注册技术协调会
(ICH)质量风险管理指南Q9(R1)的修订工作。
三、加强质量体系建设,启动省级机构评估
(一)质量管理体系建设工作
质量管理体系通过对工作过程进行有效地管理和控制,以过程管理方法进行系统管理,不断促进工作质量的提升。核查中心一直以来非
常重视质量管理体系建设,每年制定质量管理体系审核计划,按照工作要求开展内部审核和外部监督审核。2021年12月,核查中心接受质
量管理体系再认证审核并通过。
2021年,核查中心制定了《检查工作质量评估管理规定(试行)》和《检查工作质量评估程序(试行)》。2021年12月,组织开展
2021年度检查工作质量评估,评估组专家从2021年度完成的检查任务中随机抽取10个任务,按照评估指标,对程序文件、检查方案、现
场检查实施、检查报告、检查报告审核(会审)、检查时限等六个方面进行评估,并完成评估报告。检查工作质量评估工作为各部门提升
质量意识,促进质量管理体系有效运行,提高检查工作质量发挥了积极作用。
(二)启动省级药品检查机构评估工作
按照国家药监局工作部署及《药品生产监督管理办法》相关要求,核查中心负责对省级药品检查机构质量管理体系进行指导和评估。
2021年,核查中心开展省级药品检查机构质量管理体系摸底调查,初步完成省级药品检查机构评估工作方案和评估指标体系,并将在
2022年开展试点评估工作。
四、整合信息技术资源,加大信息公开力度
核查中心已建成覆盖药品检查核查全生命周期的流程管理系统,以及公文管理、质量体系文件管理、人力资源管理、信息知识管理等综
合应用系统。开发了核查中心网站(中文/英文)、微信公众号“CFDI检查核查之窗”、药品注册申请人之窗等信息公开和交流平台,为核
查中心的检查任务管理和信息公开工作提供信息技术支持。
2021年,药品注册申请人之窗正式上线运行,平台整合了药品注册生产现场核查等6个核查任务类型,扩大现场核查信息公开力度,拓
宽核查中心与申请人之间的信息交互渠道,提升了检查核查工作效率和服务质量。截至12月31日,平台注册用户已达2229个。
2021年,核查中心中英文网站主动公开信息1092条,网站浏览量约444万余次;微信公众号发布信息208条,阅读量44.5万次,关注人
数超过4.4万人。
五、努力推动队伍建设,全力提升队伍水平
2021年,核查中心继续落实《国务院办公厅关于建立职业化专业化药品检查员队伍的意见》《国家药监局关于加快推进职业化专业化药
品检查员队伍的实施意见》的要求,全力推进职业化专业化检查员队伍建设。在国家药监局相关司局的指导下,起草了《职业化专业化药品
检查员分级分类管理办法》《职业化专业化药品检查员教育培训管理办法》等6个文件,并已印发执行。
为强化组织保障,加强统筹协调,核查中心制定《高水平检查员培养工作规划》,对药品检查员能力提升进行谋划,明确检查员队伍建
设及能力提升的目标方向、工作措施和具体要求,形成《国家药监局核查中心药品检查先锋“百人计划”实施工作方案》,计划遴选出个
人素质高、工作作风好、检查能力强的优秀检查员,为其搭建更多的沟通交流平台,组织多层次、多形式、多元化的研讨和实训,加快建
设一支政治过硬、素质优良、业务精湛、廉洁高效的检查员队伍。
2021年,核查中心努力克服疫情影响,采取多种形式开展检查员培训,举办各类检查员培训26期,组织20余次内部培训和经验分享会,
持续提升检查员的检查能力,完成9家实训基地的考察评估工作,与7家实训基地签订合作协议,将为检查员提供更具针对性的现场实践培
训机会。
六、积极参与国际交流,做好NRA评估准备
2021年9月,国家药监局申请启动预加入药品检查合作计划(PIC/S)程序,核查中心成立工作专班,完成加入PIC/S预申请材料。积极
参与PIC/S组织的相关线上国际会议,了解PIC/S组织的工作模式及最新的工作动态,讨论分享问题见解。同时,根据加入PIC/S的工作要求
,认真做好药品检查标准对标工作,与PIC/S工作领导小组办公室积极沟通,梳理和组织翻译需要报送的各类文件。
2021年,按照国家药监局疫苗NRA评估工作部署,核查中心积极做好世界卫生组织(WHO)疫苗国家监管检查模块GCP、GMP(国家
级层面)部分评估准备工作,加强与WHO沟通协调,梳理总结有关工作情况,持续推进质量管理体系完善。
七、结语
药品监管关系公众用药健康,药品检查核查工作贯穿药品的全生命周期,为国家药品监管工作提供重要支撑,为保障药品安全提供重要保
证,为促进公众用药健康、建设健康中国、增进人民福祉发挥积极作用。
2021年,核查中心积极投入新冠肺炎疫情防控和物资保障工作,努力克服疫情困难,承担高强度的检查核查工作,获得了中央和国家机
关工委、市场监管总局和国家药监局多项集体荣誉和个人表彰,进一步筑牢了为药品检查事业不懈奋斗的信心和决心。
2022年,核查中心将在国家药监局的统一领导下,继续牢记初心使命,坚决贯彻落实全国药品监督管理暨党风廉政建设等工作会议精神
,继续推进药品注册核查工作,不断强化疫苗巡查和血液制品巡查,持续开展监督检查和有因检查,积极参与NRA评估和加入PIC/S 等国际
交流相关工作,持续加强检查员职业化专业化队伍建设,坚守药品安全的底线,全力推动药品检查工作高质量发展,做好人民健康的忠诚卫
士。
国家药品监督管理局
食品药品审核查验中心
2022年6月26日
前期,国家药监局发布了《药品信息化追溯体系建设导则》《药品追溯码编码要求》等10个药品追溯标准规范,获得了行业的广泛关
注。在标准实施过程中,业界对药品追溯码的标识、药品追溯信息查询显示等部分实施细节存在不同的理解和做法。为从技术实施角度指
导药品上市许可持有人和生产企业开展药品追溯相关工作,在国家药监局药品注册司、药品监管司的指导下,国家药监局信息中心组织编
制了《药品追溯码标识规范》《药品追溯消费者查询结果显示规范》2个标准。
2.制定《药品追溯码标识规范》《药品追溯消费者查询结果显示规范》2个标准的依据有哪些?标准的编制严格依据《中华人民共和国药品管理法》《药品生产监督管理办法》《药品注册管理办法》《药品说明书和标签管理规
定》《关于药品信息化追溯体系建设的指导意见》(国药监药管〔2018〕35号)等相关法律法规,遵循《重要产品追溯 追溯体系通用要
求》等国家标准以及我局已发布的药品追溯标准。
二、标准的主要内容《药品追溯码标识规范》规定了药品追溯码标识的原则、一般要求、样式要求、位置要求和质量要求,适用于规范和指导药品上市许
可持有人和生产企业在中国境内销售和使用药品的各级销售包装单元上以印刷、粘贴等方式进行药品追溯码的标识。
4.《药品追溯消费者查询结果显示规范》的主要内容有哪些?适用于什么情况?《药品追溯消费者查询结果显示规范》规定了通过药品追溯码在药品追溯系统查询到的药品追溯信息结果的总体要求、显示方式要求
和显示内容要求,适用于规范和指导药品上市许可持有人和生产企业通过药品追溯系统向消费者提供的药品追溯信息查询结果。
三、有关内容的说明药品追溯码标识的内容应包括“药品追溯码”字样、药品追溯码人眼识读的字符和药品追溯码设备识读的符号(一般包括一维条码或
二维码)。
7.药品追溯码标识原则有哪些?药品追溯码标识原则包括:一是易识别性,药品追溯码标识应保证能够被使用者和相关设备方便、准确地识读。二是清晰性,药品追
溯码标识应保证图像清晰、颜色与底色对比分明。三是显著性,药品追溯码应标识在明显可见之处,便于使用者快速寻找和定位。
8.药品追溯码标识的一般要求有哪些?药品追溯码标识的一般要求包括:一是药品追溯码标识应符合国家相关法律法规和标准的要求。二是药品追溯码标识应清晰可读,可
被扫码设备和人眼识读。
9.如何在药品大包装标识药品追溯码?为方便药品大包装堆放时的扫描作业,在药品大包装标识药品追溯码时,宜在2个及以上的平面上标识,企业可结合储运具体情况,
选择不同的平面标识药品追溯码。
10.在反光材质、热缩膜等特殊包装材质上标识药品追溯码时,应注意哪些问题?在特殊包装材质上标识药品追溯码时,应充分考虑包装材质对药品追溯码识读造成的影响,确保药品追溯码可识读。如在反光材质的
包装上标识药品追溯码时,应采取相应措施消除反光对药品追溯码识读(包括人眼和设备识读)造成的影响;在热缩膜上标识一维条码
时,应充分衡量并克服变形对一维条码识读(包括人眼和设备识读)造成的影响,一维条码的条方向应与热缩膜的缩率最大的方向一致。
11.药品追溯消费者查询结果显示的总体要求有哪些?药品追溯消费者查询结果显示的总体要求包括:一是通过药品追溯码在药品追溯系统查询到的药品追溯信息结果应符合国家相关法律
法规和标准的要求。二是通过药品追溯码在药品追溯系统查询到的药品追溯信息应与药品实际情况一致。
12. 药品追溯消费者查询结果显示方式要求有哪些?为便于消费者查询和避免引起误导,药品追溯系统提供的查询结果应直接显示药品追溯信息,包含“药品追溯信息”字样,并应在显
著位置告知本次查询结果的药品追溯信息提供方,推荐采用“本追溯信息由××××(上市许可持有人)授权本追溯系统提供”字样。
近年来,放射性体内治疗药物的研发进入了快速发展阶段。放射性药物是一类特殊的药物,其临床研发与非放射性药物存在一定的差
异。为更好的推动和指导申办者在放射性治疗药物领域的临床研发、明确技术标准,我们结合国内外放射性治疗药物研发经验,借鉴国际相
关技术要求制定本指导原则。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起一个
月。
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年6月28日
随着经济快速发展和生活方式的改变,我国2型糖尿病的患病率具有逐年升高趋势。2型糖尿病的并发症是影响患者生活质量甚至生存的
最重要因素,给患者及和社会带来了沉重负担。虽然当前可选择的降糖药物种类较多,但仍然存在未被满足的临床需求。
结合2型糖尿病疾病特征、临床实践变化以及药物临床研发进展,为进一步对当前2型糖尿病降糖药物临床试验设计提供建议和参考,药
审中心组织撰写了《成人2型糖尿病药物临床研发技术指导原则》,形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年6月27日
为指导药物临床试验申办者规范开展临床试验期间方案变更相关工作,在国家药品监督管理局的部署下,药审中心组织制定了《药物临
床试验期间方案变更技术指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综
药管〔2020〕9号)要求,经国家药品监督管理局审核同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年6月23日
为不断丰富完善仿制药个药指导原则并持续推进一致性评价工作,进一步规范他达拉非片、氯雷他定片和富马酸丙酚替诺福韦片的生物
等效性研究,经广泛调研和讨论,我中心组织起草了《他达拉非片生物等效性研究指导原则(征求意见稿)》等三项技术指导原则。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,以便后续完善。征求意见时限为自发布之日起1个月。
国家药品监督管理局药品审评中心
2022年6月22日
慢性淋巴细胞白血病(Chronic lymphocytic leukemia,CLL)是一种主要发生在中老年人群的成熟B淋巴细胞克隆增殖性肿瘤,其总
体发病率因社会老龄化程度的加深呈增高趋势。在过去的20年里,CLL的治疗选择不断增加,治疗理念和临床实践正在快速发生变化,患者
的生存时间和无进展生存时间不断得到延长。同时,由于CLL的惰性特征和高发于老年人的特点,相比其他恶性肿瘤,CLL新药临床试验在
设计和执行中需要更加关注患者的治疗目标和需求,以在保持和改善患者生活质量与传统抗肿瘤治疗理念之间达到平衡。为进一步明确技术
标准,使CLL适应症的新药研发人员更准确地把握疾病特征,并推动以患者为核心的新药研发理念,在临床试验设计和执行过程中更深入地
关注和了解患者的需求,我中心组织起草了《慢性淋巴细胞白血病新药临床研发技术指导原则》,经中心内部讨论,并征求部分专家意见
,现形成征求意见稿。
国家药品监督管理局药品审评中心
2022年6月20日
单臂临床试验的研发策略显著地缩短了新药的上市时间;特别是近年来,许多新药在临床研究早期阶段就显现出非常突出的有效性数据,因此,越来越多的研发企业希望采用单臂临床试验支持抗肿瘤药物的上市申请。但与公认的金标准随机对照研究结果相比,单臂临床试验的结果用于新药的获益与风险评估具有一定的不确定性。
为了阐明当前对单臂临床试验用于支持抗肿瘤药上市申请适用性的科学认识,以期指导企业在完成早期研究后,更好地评估是否适合开展单臂临床试验作为关键临床研究用以支持后续的上市申请,药审中心组织撰写了《单臂临床试验用于支持抗肿瘤药上市申请的适用性技术指导原则》,形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个月。
国家药品监督管理局药品审评中心
2022年6月20日
儿童因其生理和心理发育特点,在不良感觉的耐受性方面有别于成人,口感不佳所导致的不良用药行为风险也相应增高,因此,儿童用
药口感评价具有重要的临床意义与价值。在2020年12月发布的《儿童用药(化学药品)药学开发指导原则(试行)》(2020年第67号)
中,已提出口感评价在儿童用药研制中的重要意义。为进一步鼓励儿童用药研发生产,满足儿童用药需求,保障儿童用药安全。我中心组织
撰写了《儿童用药口感设计与评价的技术指导原则》。
国家药品监督管理局药品审评中心
2022年6月17日
为推动构建中医药理论、人用经验和临床试验相结合的中药注册审评证据体系,引导申请人按照“三结合”注册审评证据体系研发符合
中医药治疗优势和特点的、用于慢性胃炎、胃食管反流病的中药新药,药审中心组织行业专家起草了《中药新药用于慢性胃炎的临床疗效评
价指导原则(征求意见稿)》《中药新药用于胃食管反流病的临床疗效评价指导原则(征求意见稿)》,经中心内部讨论并组织学术界、工
业界专家研讨,已形成征求意见稿。现在中心网站予以公示,以广泛听取各界意见和建议。
感谢您的参与和大力支持!
药品审评中心
2022年4月29日
基于当前利拉鲁肽在我国的实际情况和企业的临床研发需求,在国家药品监督管理局的部署下,药审中心组织制定了《利拉鲁肽用于体
重管理的临床试验设计指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管
〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年1月21日
为全面掌握中国新药注册临床试验进展,运用信息化手段提升药品监管能力,及时对外公开临床试验进展信息,为新药研发、资源配置
和药品审评审批提供参考,药审中心根据药物临床试验登记与信息公示平台的新药临床试验登记信息,对2021年中国新药注册临床试验现状
进行了全面汇总和分析,编制了《中国新药注册临床试验进展年度报告(2021年)》。
本次年度报告主要根据2021年度登记的药物临床试验信息,从药物类型、品种及靶点特征、适应症、申办者类型、注册分类、试验分
类、试验分期、特殊人群试验、临床试验组长单位、启动耗时和完成情况等角度对临床试验的总体趋势变化、主要特点、突出问题等进行汇
总分析,同时对比近三年临床试验登记数据,对近年来的趋势特征进行总结分析。
国家药监局药审中心
2022年6月7日
为规范和指导特异性人免疫球蛋白的研发、生产和注册,进一步明确技术评价标准,在国家药品监督管理局的部署下,药审中心组织制
定了《特异性人免疫球蛋白药学研究与评价技术指导原则》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年5月20日
为规范和指导体外基因修饰系统的药学研究,在国家药品监督管理局的部署下,药审中心组织制定了《体外基因修饰系统药学研究与评
价技术指导原则(试行)》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年5月26日
为鼓励罕见疾病药物研发,从临床研究方法学角度指导申办者提高研发效率,药审中心组织制定了《罕见疾病药物临床研究统计学指导原则
(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家
药品监督管理局审查同意,现予发布,自发布之日起实施。
特此通告。
国家药监局药审中心
2022年6月2日
为规范和指导免疫细胞治疗产品的药学研发、生产和注册,在国家药品监督管理局的部署下,药审中心组织制定了《免疫细胞治疗产品
药学研究与评价技术指导原则(试行)》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年5月26日
为规范和指导体内基因治疗产品的药学研发、生产和注册,在国家药品监督管理局的部署下,药审中心组织制定了《体内基因治疗产品
药学研究与评价技术指导原则(试行)》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年5月26日
局部给药局部起效药物剂型众多、辅料复杂、给药途径多样,与系统给药药物相比,其在临床试验设计和审评评价方面存在特殊性,且面临较大困难和挑战。为进一步指导业界、研究者和监管机构在该领域药物的科学研发和评价,药审中心组织起草了《局部给药局部起效药物临床试验技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号),经国家药品监督管理局审查同意,现予发布。
特此通告。
国家药监局药审中心
2022年5月26日
肿瘤免疫治疗是当前抗肿瘤新药研发的热点,如何提高免疫相关不良事件识别、判定的科学性和稳健性,提高说明书撰写质量,切实保
障患者用药安全,是目前监管方及业界亟需解决的问题。在国家药品监督管理局的部署下,药审中心组织制定了《抗肿瘤治疗的免疫相关不
良事件评价技术指导原则》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年5月16日
随着各种诊疗技术的进步和人民对“舒适医疗”的要求不断提高,麻醉学科对各种临床手术、操作的支持越来越重要。目前,临床已有
一些静脉全身麻醉药广泛应用,但仍存在对于具有更理想的有效性和安全性特征的创新药物的临床需求。为规范创新静脉全身麻醉药的临床
研究,在国家药品监督管理局的部署下,药审中心组织制定了《静脉全身麻醉药的临床评价技术指导原则》(见附件),供药品研发企业和
临床研究单位参考。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年5月20日
根据《药品注册管理办法》(国家市场监督管理总局令第27号),为规范申报资料的提交,在国家药监局的部署下,药审中心组织制定
了《化学药品及生物制品说明书通用格式和撰写指南》(见附件),经国家药监局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年5月20日
北京时间2022年5月19日,世界卫生组织在官网发布信息,正式将康希诺生物股份公司重组新型冠状病毒疫苗(5型腺病毒载体)列入其
紧急使用清单,该疫苗成为继国药中生北京公司新冠灭活疫苗、科兴中维公司新冠灭活疫苗后第三个被列入世卫组织紧急使用清单的国产疫苗。
国家药监局长期以来与世界卫生组织保持良好协商关系,就新冠病毒疫苗监管等相关事宜开展合作。
国家药监局网站
ICH《E11A:儿科外推》指导原则现进入第3阶段区域公开征求意见阶段。按照ICH相关章程要求,ICH的监管机构成员需收集本地区关
于第2b阶段指导原则草案的意见并反馈ICH。
E11A指导原则草案的英文原文和中文译文见附件,现就该指导原则内容及中文译文向社会公开征求意见。
社会各界如有相关建议(填写附件3),请于2022年7月30日前通过联系人电子邮件反馈我中心。
国家药品监督管理局药品审评中心
2022年4月25日
ICH《Q2(R2):分析方法验证》和《Q14:分析方法开发》指导原则现进入第3阶段区域公开征求意见阶段。按照ICH相关章程要求,
ICH的监管机构成员需收集本地区关于第2b阶段指导原则草案的意见并反馈ICH。
Q2(R2)和Q14指导原则草案的英文原文和中文译文见附件1-4。现向社会公开征求上述指导原则草案英文原文意见,指导原则内容相
关建议请填写附件5(中英文均可)。同时,为后续平稳实施Q2(R2)和Q14指导原则,本次也同步征求草案中文译文意见,中文翻译相关
建议请填写附件6。
社会各界如有相关建议,请于2022年7月15日前通过联系人电子邮箱反馈。
联系人:田洁、曾繁旭
邮箱:tianj@cde.org.cn,zengfx@cde.org.cn
国家药品监督管理局药品审评中心
2022年4月25日
经国家药品监督管理局仿制药质量和疗效一致性评价专家委员会审核确定,现发布仿制药参比制剂目录(第五十三批)。
特此通告。
附件:仿制药参比制剂目录(第五十三批)
国家药监局
2022年4月22日
随着抗肿瘤药物研发的进展,越来越多的研究表明,一种药物可以应用于不同瘤种、同一瘤种的不同阶段或人群,还可以与不同作用机
制的药物联合。药品说明书是药品安全性信息最主要的载体,是指导安全、合理使用药品的重要法定文件。在一种药物单药以及联合用药积
累了大量的安全性数据的情况下,面对不同的使用者,如何科学、全面、清晰、简洁、易读的在说明书中呈现药物在不同使用场景下的安全
性特征,切实保障患者用药安全,是目前监管方及业界亟需解决的问题。在国家药品监督管理局的部署下,药审中心组织制定了《抗肿瘤药
物说明书不良反应数据汇总指导原则》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。
特此通告。
附件:抗肿瘤药物说明书不良反应数据汇总指导原则
国家药监局药审中心
2022年4月19日
为推动解决我国儿科临床普遍存在的说明书儿童用药信息增补或修订滞后的问题,规范由国家儿科专业协会或国家儿童医学中心针对我
国儿科临床需求迫切的药品提出的修订说明书增补儿童用药信息的申请处理流程,确保说明书修订的质量和效率,药审中心起草了《已上市
药品说明书增补儿童用药信息工作程序》及《药审中心关于已上市药品说明书增补儿童用药信息的工作流程》。
现公开征求社会各界意见。征求意见时限为自发布之日起一个月。
您的反馈意见请发到以下邮箱:zhanghao@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年4月21日
药物临床依赖性研究是具有潜在滥用风险的新药上市前的重要研究内容,我国尚无专门技术要求对此类研究进行规范管理。为此,药审
中心起草了《药物临床依赖性研究技术指导原则》。经征求中心内部各相关专业及部分具有药物临床依赖性研究经验的专家及企业意见,形
成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起一个
月。
您的反馈意见请发到以下邮箱:
联系方式:zhanghao@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年4月18日
各省、自治区、直辖市和新疆生产建设兵团药品监督管理局:
为落实《中华人民共和国药品管理法》《中华人民共和国疫苗管理法》有关建立药物警戒制度的要求,指导药品监督管理部门科学规范
开展药物警戒检查工作,国家药监局组织制定了《药物警戒检查指导原则》,现予印发,请遵照执行,并就有关工作要求通知如下:
一、 各省级药品监督管理部门要强化组织领导和统筹协调,建立健全工作机制,推进药物警戒体系和能力建设,全面加强药物警戒各项
工作。
二、 各省级药品监督管理部门要督促指导本行政区域内药品上市许可持有人进一步完善药物警戒体系,规范开展药物警戒活动,确保持
续符合《药物警戒质量管理规范》,切实履行药物警戒主体责任。
三、 各省级药品监督管理部门要结合本行政区域监管实际,在日常监管工作中纳入药物警戒检查相关内容,科学制定检查计划,有序高
效组织实施,工作中可进一步细化相关工作内容、完善相关工作要求,切实落实属地监管责任。
四、 本《药物警戒检查指导原则》自发布之日起施行,原国家食品药品监管总局于2015年7月2日印发的《食品药品监管总局关于印发
药品不良反应报告和监测检查指南(试行)的通知》(食药监药化监〔2015〕78号)同时废止。
国家药监局
2022年4月11日
国家药品监督管理局药品审评中心2021年2月发布了《已上市化学药品药学变更研究技术指导原则(试行)》,规定口服固体制剂的多
种药学变更情形(如重大变更、中等变更、部分微小变更及增加规格等)均需进行变更前后的溶出曲线对比研究,研究结果关系到变更分类
的界定以及是否能够豁免生物等效性研究。为更好的指导企业进行药学变更研究,统一技术要求,我中心经调研以及与专家和业界讨论,组
织起草了《〈已上市化学药品药学变更研究技术指导原则(试行)〉中溶出曲线研究条件的问答(征求意见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
请将您的反馈意见发到以下联系人的邮箱。
联系人:王淑华;姜典卓
邮箱:wangshuhua@cde.org.cn;jiangdzh@cde.org.cn
感谢您的参与和大力支持。
药品审评中心
2022年4月7日
各省、自治区、直辖市和新疆生产建设兵团药品监督管理局:
为贯彻落实《药品管理法》及《药品注册管理办法》《药品生产监督管理办法》有关要求,进一步指导药品上市许可持有人(以下简
称持有人)建立年度报告制度,国家药监局组织制定了《药品年度报告管理规定》(见附件1)和《药品年度报告模板》(见附件2),现
予印发。同时,为保障药品年度报告制度的落地实施,国家药监局建设了药品年度报告采集模块,同期启用。现将有关事项通知如下:
一、 督促持有人落实药品年度报告的主体责任
药品年度报告制度是《药品管理法》提出的一项新制度。《药品管理法》明确规定,药品上市许可持有人应当建立年度报告制度,每
年将药品生产销售、上市后研究、风险管理等情况按照规定向省、自治区、直辖市人民政府药品监督管理部门报告。年度报告填报主体为
持有人;持有人为境外企业的,由其依法指定的、在中国境内承担连带责任的企业法人履行年度报告义务。
各省级药品监管部门要加强政策宣传和监督指导,通过规范持有人的年度报告行为,进一步督促持有人落实全过程质量管理主体责任。
持有人应当以年度报告为抓手,增强主体责任意识,发挥主观能动性,进一步提升自身管理水平。持有人应当指定专人负责年度报告工作,
完善内部报告管理制度,对年度报告的内容严格审核把关,确保填报信息真实、准确、完整和可追溯。
二、 切实做好数据共享和信息应用
国家药监局已经建设了药品年度报告采集模块。为方便持有人填报,该模块直接对接药品监管数据共享平台的药品注册、药品生产许可
等有关信息,实现了关键基础信息自动带出,有助于提高填报信息的准确性。后续,还将充分发挥国家药品监管数据共享平台优势,逐步将
年度报告信息分别归集纳入药品品种档案、药品安全信用档案,夯实药品智慧监管的信息基础。
各省级药品监管部门要将年度报告信息作为监督检查、风险评估、信用监管等工作的参考材料和研判依据,逐步实现精准监管、科学监
管,提升药品全生命周期监管效能。同时,结合监督检查等工作安排,对持有人年度报告内容进行审核,对不按规定进行年度报告的持有人
依法查处,并纳入药品安全信用档案。
三、 全力做好年度报告采集模块的运行维护
药品年度报告采集模块分为企业端和监管端。企业端采集信息包括公共部分和产品部分两方面内容。其中,公共部分包括持有人信息、
持有产品总体情况、质量管理概述、药物警戒体系建设及运行情况、接受境外委托加工情况、接受境外药品监管机构检查情况等六个方面内
容;产品部分包括产品基础信息、生产销售情况、上市后研究及变更管理情况、风险管理情况等四个方面内容。持有人完成药品年度报告的
填报并提交后,省级药品监管部门可以通过监管端查看本行政区域内持有人的药品年度报告信息。
国家药监局信息中心要做好模块上线后的技术支持工作。企业端和监管端的权限开通及操作流程可参考操作手册(见附3和附4)。最新
电子版操作手册可从系统中下载。若在系统使用过程中发现问题,用户可随时联系技术支持客服热线(4006676909转2);亦可通过加入
QQ工作群(监管用户:320404770;企业用户:282253676)进行沟通联络。
四、其他事项
1.本规定自发布之日起施行,药品年度报告采集模块同时启用。
2.鉴于我国首次实施药品年度报告制度,药品年度报告采集模块尚处于试运行阶段,2021年度报告信息填报时间截止为2022年8月31日
;从明年开始,每年4月30日之前填报上一年度报告信息。
国家药监局
2022年4月11日
2022年4月11日
为规范和指导胰岛素类产品生物类似药的研发、生产和注册,进一步明确技术评价标准,在国家药品监督管理局的部署下,药审中心组
织制定了《胰岛素类产品生物类似药药学研究与评价技术指导原则》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。
特此通告。
附件:胰岛素类产品生物类似药药学研究与评价技术指导原则
国家药监局药审中心
2022年3月10日
生物制药技术的发展,推动双特异性抗体类药物进入高速发展阶段,尤其是在肿瘤治疗领域,双特异性抗体类药物的研发持续增长。
为了对双特异性抗体类抗肿瘤药物的临床研发中,需要特殊关注的问题提出建议,并指导企业开展更为科学的临床研发,药品审评中心
组织撰写了《双特异性抗体类抗肿瘤药物临床研发技术指导原则》,形成征求意见稿,供药物研发相关人员参考。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:唐凌,宋媛媛
联系方式:tangl@cde.org.cn,songyy@cde.org.cn
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年4月11日
近期,国内本土疫情发展迅速,北京疫情防控仍面临境外输入、京外输入双重风险。基于疫情防控需要,2022年1月29日中心网站发布
《药审中心关于疫情期间调整受理工作方式及接收申报资料要求的通知》(以下简称《通知》),明确邮包及内部申报资料消杀、核酸检测
等要求。为进一步落实疫情防控政策要求,严防严控疫情期间申报资料接收“物传人”风险,现就有关要求通知如下:
一、外地进(返)京人员本人及其共同工作、生活人员请暂勿现场办理。对于确需到现场办理的京内低风险区域人员,须主动出示行程
码、“北京健康宝”绿码和48小时内核酸检测阴性证明,通过申请人之窗网上预约方式进行预约登记。不符合北京疫情防控相关政策的人
员,请暂不现场办理业务。
二、为严控疫情风险,降低人员聚集交叉感染风险,鼓励申请人采用邮寄方式递交申报资料。申请人递交申报资料需符合《通知》相关
要求,有关资料接收的共性问题及细节要求请遵照下列附件执行。
药品审评中心
2022年4月7日
为贯彻实施《中华人民共和国药品管理法》《中华人民共和国疫苗管理法》,全面落实药品上市许可持有人对药品研制、生产、经营、
使用全过程中药品的安全性、有效性和质量可控性的主体责任,进一步规范对药品上市许可持有人的监督检查工作,国家药监局组织起草了
《药品上市许可持有人检查要点(征求意见稿)》,现向社会公开征求意见。请于2022年4月30日前,将有关意见通过电子邮件反馈至
ypjgs@nmpa.gov.cn,邮件标题请注明“持有人检查要点意见反馈”。
国家药监局综合司
2022年3月28日
国家市场监督管理总局令
第27号
《药品注册管理办法》已于2020年1月15日经国家市场监督管理总局2020年第1次局务会议审议通过,现予公布,自2020年7月1日
起施行。
局长 肖亚庆
2020年1月22日
药品注册管理办法
(2020年1月22日国家市场监督管理总局令第27号公布)
第一章 总 则
第一条 为规范药品注册行为,保证药品的安全、有效和质量可控,根据《中华人民共和国药品管理法》(以下简称《药品管理
法》)、《中华人民共和国中医药法》、《中华人民共和国疫苗管理法》(以下简称《疫苗管理法》)、《中华人民共和国行政许可
法》、《中华人民共和国药品管理法实施条例》等法律、行政法规,制定本办法。
第二条 在中华人民共和国境内以药品上市为目的,从事药品研制、注册及监督管理活动,适用本办法。
第三条 药品注册是指药品注册申请人(以下简称申请人)依照法定程序和相关要求提出药物临床试验、药品上市许可、再注册等申
请以及补充申请,药品监督管理部门基于法律法规和现有科学认知进行安全性、有效性和质量可控性等审查,决定是否同意其申请的活
动。
申请人取得药品注册证书后,为药品上市许可持有人(以下简称持有人)。
第四条 药品注册按照中药、化学药和生物制品等进行分类注册管理。
中药注册按照中药创新药、中药改良型新药、古代经典名方中药复方制剂、同名同方药等进行分类。
化学药注册按照化学药创新药、化学药改良型新药、仿制药等进行分类。
生物制品注册按照生物制品创新药、生物制品改良型新药、已上市生物制品(含生物类似药)等进行分类。
中药、化学药和生物制品等药品的细化分类和相应的申报资料要求,由国家药品监督管理局根据注册药品的产品特性、创新程度和审
评管理需要组织制定,并向社会公布。
境外生产药品的注册申请,按照药品的细化分类和相应的申报资料要求执行。
第五条 国家药品监督管理局主管全国药品注册管理工作,负责建立药品注册管理工作体系和制度,制定药品注册管理规范,依法组
织药品注册审评审批以及相关的监督管理工作。国家药品监督管理局药品审评中心(以下简称药品审评中心)负责药物临床试验申请、药
品上市许可申请、补充申请和境外生产药品再注册申请等的审评。中国食品药品检定研究院(以下简称中检院)、国家药典委员会(以下
简称药典委)、国家药品监督管理局食品药品审核查验中心(以下简称药品核查中心)、国家药品监督管理局药品评价中心(以下简称药
品评价中心)、国家药品监督管理局行政事项受理服务和投诉举报中心、国家药品监督管理局信息中心(以下简称信息中心)等药品专业
技术机构,承担依法实施药品注册管理所需的药品注册检验、通用名称核准、核查、监测与评价、制证送达以及相应的信息化建设与管理
等相关工作。
第六条 省、自治区、直辖市药品监督管理部门负责本行政区域内以下药品注册相关管理工作:
(一)境内生产药品再注册申请的受理、审查和审批;
(二)药品上市后变更的备案、报告事项管理;
(三)组织对药物非临床安全性评价研究机构、药物临床试验机构的日常监管及违法行为的查处;
(四)参与国家药品监督管理局组织的药品注册核查、检验等工作;
(五)国家药品监督管理局委托实施的药品注册相关事项。
省、自治区、直辖市药品监督管理部门设置或者指定的药品专业技术机构,承担依法实施药品监督管理所需的审评、检验、核查、监
测与评价等工作。
第七条 药品注册管理遵循公开、公平、公正原则,以临床价值为导向,鼓励研究和创制新药,积极推动仿制药发展。
国家药品监督管理局持续推进审评审批制度改革,优化审评审批程序,提高审评审批效率,建立以审评为主导,检验、核查、监测与
评价等为支撑的药品注册管理体系。
第二章 基本制度和要求
第八条 从事药物研制和药品注册活动,应当遵守有关法律、法规、规章、标准和规范;参照相关技术指导原则,采用其他评价方法
和技术的,应当证明其科学性、适用性;应当保证全过程信息真实、准确、完整和可追溯。
药品应当符合国家药品标准和经国家药品监督管理局核准的药品质量标准。经国家药品监督管理局核准的药品质量标准,为药品注册
标准。药品注册标准应当符合《中华人民共和国药典》通用技术要求,不得低于《中华人民共和国药典》的规定。申报注册品种的检测项
目或者指标不适用《中华人民共和国药典》的,申请人应当提供充分的支持性数据。
药品审评中心等专业技术机构,应当根据科学进展、行业发展实际和药品监督管理工作需要制定技术指导原则和程序,并向社会公
布。
第九条 申请人应当为能够承担相应法律责任的企业或者药品研制机构等。境外申请人应当指定中国境内的企业法人办理相关药品注
册事项。
第十条 申请人在申请药品上市注册前,应当完成药学、药理毒理学和药物临床试验等相关研究工作。药物非临床安全性评价研究应
当在经过药物非临床研究质量管理规范认证的机构开展,并遵守药物非临床研究质量管理规范。药物临床试验应当经批准,其中生物等效
性试验应当备案;药物临床试验应当在符合相关规定的药物临床试验机构开展,并遵守药物临床试验质量管理规范。
申请药品注册,应当提供真实、充分、可靠的数据、资料和样品,证明药品的安全性、有效性和质量可控性。
使用境外研究资料和数据支持药品注册的,其来源、研究机构或者实验室条件、质量体系要求及其他管理条件等应当符合国际人用药
品注册技术要求协调会通行原则,并符合我国药品注册管理的相关要求。
第十一条 变更原药品注册批准证明文件及其附件所载明的事项或者内容的,申请人应当按照规定,参照相关技术指导原则,对药品
变更进行充分研究和验证,充分评估变更可能对药品安全性、有效性和质量可控性的影响,按照变更程序提出补充申请、备案或者报告。
第十二条 药品注册证书有效期为五年,药品注册证书有效期内持有人应当持续保证上市药品的安全性、有效性和质量可控性,并在
有效期届满前六个月申请药品再注册。
第十三条 国家药品监督管理局建立药品加快上市注册制度,支持以临床价值为导向的药物创新。对符合条件的药品注册申请,申请
人可以申请适用突破性治疗药物、附条件批准、优先审评审批及特别审批程序。在药品研制和注册过程中,药品监督管理部门及其专业技
术机构给予必要的技术指导、沟通交流、优先配置资源、缩短审评时限等政策和技术支持。
第十四条 国家药品监督管理局建立化学原料药、辅料及直接接触药品的包装材料和容器关联审评审批制度。在审批药品制剂时,对
化学原料药一并审评审批,对相关辅料、直接接触药品的包装材料和容器一并审评。药品审评中心建立化学原料药、辅料及直接接触药品
的包装材料和容器信息登记平台,对相关登记信息进行公示,供相关申请人或者持有人选择,并在相关药品制剂注册申请审评时关联审
评。
第十五条 处方药和非处方药实行分类注册和转换管理。药品审评中心根据非处方药的特点,制定非处方药上市注册相关技术指导原
则和程序,并向社会公布。药品评价中心制定处方药和非处方药上市后转换相关技术要求和程序,并向社会公布。
第十六条 申请人在药物临床试验申请前、药物临床试验过程中以及药品上市许可申请前等关键阶段,可以就重大问题与药品审评中
心等专业技术机构进行沟通交流。药品注册过程中,药品审评中心等专业技术机构可以根据工作需要组织与申请人进行沟通交流。
沟通交流的程序、要求和时限,由药品审评中心等专业技术机构依照职能分别制定,并向社会公布。
第十七条 药品审评中心等专业技术机构根据工作需要建立专家咨询制度,成立专家咨询委员会,在审评、核查、检验、通用名称核
准等过程中就重大问题听取专家意见,充分发挥专家的技术支撑作用。
第十八条 国家药品监督管理局建立收载新批准上市以及通过仿制药质量和疗效一致性评价的化学药品目录集,载明药品名称、活性
成分、剂型、规格、是否为参比制剂、持有人等相关信息,及时更新并向社会公开。化学药品目录集收载程序和要求,由药品审评中心制
定,并向社会公布。
第十九条 国家药品监督管理局支持中药传承和创新,建立和完善符合中药特点的注册管理制度和技术评价体系,鼓励运用现代科学
技术和传统研究方法研制中药,加强中药质量控制,提高中药临床试验水平。
中药注册申请,申请人应当进行临床价值和资源评估,突出以临床价值为导向,促进资源可持续利用。
第三章 药品上市注册
第一节 药物临床试验
第二十条 本办法所称药物临床试验是指以药品上市注册为目的,为确定药物安全性与有效性在人体开展的药物研究。
第二十一条 药物临床试验分为Ⅰ期临床试验、Ⅱ期临床试验、Ⅲ期临床试验、Ⅳ期临床试验以及生物等效性试验。根据药物特点和
研究目的,研究内容包括临床药理学研究、探索性临床试验、确证性临床试验和上市后研究。
第二十二条 药物临床试验应当在具备相应条件并按规定备案的药物临床试验机构开展。其中,疫苗临床试验应当由符合国家药品监
督管理局和国家卫生健康委员会规定条件的三级医疗机构或者省级以上疾病预防控制机构实施或者组织实施。
第二十三条 申请人完成支持药物临床试验的药学、药理毒理学等研究后,提出药物临床试验申请的,应当按照申报资料要求提交相
关研究资料。经形式审查,申报资料符合要求的,予以受理。药品审评中心应当组织药学、医学和其他技术人员对已受理的药物临床试验
申请进行审评。对药物临床试验申请应当自受理之日起六十日内决定是否同意开展,并通过药品审评中心网站通知申请人审批结果;逾期
未通知的,视为同意,申请人可以按照提交的方案开展药物临床试验。
申请人获准开展药物临床试验的为药物临床试验申办者(以下简称申办者)。
第二十四条 申请人拟开展生物等效性试验的,应当按照要求在药品审评中心网站完成生物等效性试验备案后,按照备案的方案开展
相关研究工作。
第二十五条 开展药物临床试验,应当经伦理委员会审查同意。
药物临床试验用药品的管理应当符合药物临床试验质量管理规范的有关要求。
第二十六条 获准开展药物临床试验的,申办者在开展后续分期药物临床试验前,应当制定相应的药物临床试验方案,经伦理委员会
审查同意后开展,并在药品审评中心网站提交相应的药物临床试验方案和支持性资料。
第二十七条 获准开展药物临床试验的药物拟增加适应症(或者功能主治)以及增加与其他药物联合用药的,申请人应当提出新的药
物临床试验申请,经批准后方可开展新的药物临床试验。
获准上市的药品增加适应症(或者功能主治)需要开展药物临床试验的,应当提出新的药物临床试验申请。
第二十八条 申办者应当定期在药品审评中心网站提交研发期间安全性更新报告。研发期间安全性更新报告应当每年提交一次,于药
物临床试验获准后每满一年后的两个月内提交。药品审评中心可以根据审查情况,要求申办者调整报告周期。
对于药物临床试验期间出现的可疑且非预期严重不良反应和其他潜在的严重安全性风险信息,申办者应当按照相关要求及时向药品审
评中心报告。根据安全性风险严重程度,可以要求申办者采取调整药物临床试验方案、知情同意书、研究者手册等加强风险控制的措施,
必要时可以要求申办者暂停或者终止药物临床试验。
研发期间安全性更新报告的具体要求由药品审评中心制定公布。
第二十九条 药物临床试验期间,发生药物临床试验方案变更、非临床或者药学的变化或者有新发现的,申办者应当按照规定,参照
相关技术指导原则,充分评估对受试者安全的影响。
申办者评估认为不影响受试者安全的,可以直接实施并在研发期间安全性更新报告中报告。可能增加受试者安全性风险的,应当提出
补充申请。对补充申请应当自受理之日起六十日内决定是否同意,并通过药品审评中心网站通知申请人审批结果;逾期未通知的,视为同
意。
申办者发生变更的,由变更后的申办者承担药物临床试验的相关责任和义务。
第三十条 药物临床试验期间,发现存在安全性问题或者其他风险的,申办者应当及时调整临床试验方案、暂停或者终止临床试验,
并向药品审评中心报告。
有下列情形之一的,可以要求申办者调整药物临床试验方案、暂停或者终止药物临床试验:
(一)伦理委员会未履行职责的;
(二)不能有效保证受试者安全的;
(三)申办者未按照要求提交研发期间安全性更新报告的;
(四)申办者未及时处置并报告可疑且非预期严重不良反应的;
(五)有证据证明研究药物无效的;
(六)临床试验用药品出现质量问题的;
(七)药物临床试验过程中弄虚作假的;
(八)其他违反药物临床试验质量管理规范的情形。
药物临床试验中出现大范围、非预期的严重不良反应,或者有证据证明临床试验用药品存在严重质量问题时,申办者和药物临床试验
机构应当立即停止药物临床试验。药品监督管理部门依职责可以责令调整临床试验方案、暂停或者终止药物临床试验。
第三十一条 药物临床试验被责令暂停后,申办者拟继续开展药物临床试验的,应当在完成整改后提出恢复药物临床试验的补充申
请,经审查同意后方可继续开展药物临床试验。药物临床试验暂停时间满三年且未申请并获准恢复药物临床试验的,该药物临床试验许可
自行失效。
药物临床试验终止后,拟继续开展药物临床试验的,应当重新提出药物临床试验申请。
第三十二条 药物临床试验应当在批准后三年内实施。药物临床试验申请自获准之日起,三年内未有受试者签署知情同意书的,该药
物临床试验许可自行失效。仍需实施药物临床试验的,应当重新申请。
第三十三条 申办者应当在开展药物临床试验前在药物临床试验登记与信息公示平台登记药物临床试验方案等信息。药物临床试验期
间,申办者应当持续更新登记信息,并在药物临床试验结束后登记药物临床试验结果等信息。登记信息在平台进行公示,申办者对药物临
床试验登记信息的真实性负责。
药物临床试验登记和信息公示的具体要求,由药品审评中心制定公布。
第二节 药品上市许可
第三十四条 申请人在完成支持药品上市注册的药学、药理毒理学和药物临床试验等研究,确定质量标准,完成商业规模生产工艺验
证,并做好接受药品注册核查检验的准备后,提出药品上市许可申请,按照申报资料要求提交相关研究资料。经对申报资料进行形式审
查,符合要求的,予以受理。
第三十五条 仿制药、按照药品管理的体外诊断试剂以及其他符合条件的情形,经申请人评估,认为无需或者不能开展药物临床试
验,符合豁免药物临床试验条件的,申请人可以直接提出药品上市许可申请。豁免药物临床试验的技术指导原则和有关具体要求,由药品
审评中心制定公布。
仿制药应当与参比制剂质量和疗效一致。申请人应当参照相关技术指导原则选择合理的参比制剂。
第三十六条 符合以下情形之一的,可以直接提出非处方药上市许可申请:
(一)境内已有相同活性成分、适应症(或者功能主治)、剂型、规格的非处方药上市的药品;
(二)经国家药品监督管理局确定的非处方药改变剂型或者规格,但不改变适应症(或者功能主治)、给药剂量以及给药途径的药
品;
(三)使用国家药品监督管理局确定的非处方药的活性成份组成的新的复方制剂;
(四)其他直接申报非处方药上市许可的情形。
第三十七条 申报药品拟使用的药品通用名称,未列入国家药品标准或者药品注册标准的,申请人应当在提出药品上市许可申请时同
时提出通用名称核准申请。药品上市许可申请受理后,通用名称核准相关资料转药典委,药典委核准后反馈药品审评中心。
申报药品拟使用的药品通用名称,已列入国家药品标准或者药品注册标准,药品审评中心在审评过程中认为需要核准药品通用名称
的,应当通知药典委核准通用名称并提供相关资料,药典委核准后反馈药品审评中心。
药典委在核准药品通用名称时,应当与申请人做好沟通交流,并将核准结果告知申请人。
第三十八条 药品审评中心应当组织药学、医学和其他技术人员,按要求对已受理的药品上市许可申请进行审评。
审评过程中基于风险启动药品注册核查、检验,相关技术机构应当在规定时限内完成核查、检验工作。
药品审评中心根据药品注册申报资料、核查结果、检验结果等,对药品的安全性、有效性和质量可控性等进行综合审评,非处方药还
应当转药品评价中心进行非处方药适宜性审查。
第三十九条 综合审评结论通过的,批准药品上市,发给药品注册证书。综合审评结论不通过的,作出不予批准决定。药品注册证书
载明药品批准文号、持有人、生产企业等信息。非处方药的药品注册证书还应当注明非处方药类别。
经核准的药品生产工艺、质量标准、说明书和标签作为药品注册证书的附件一并发给申请人,必要时还应当附药品上市后研究要求。
上述信息纳入药品品种档案,并根据上市后变更情况及时更新。
药品批准上市后,持有人应当按照国家药品监督管理局核准的生产工艺和质量标准生产药品,并按照药品生产质量管理规范要求进行
细化和实施。
第四十条 药品上市许可申请审评期间,发生可能影响药品安全性、有效性和质量可控性的重大变更的,申请人应当撤回原注册申
请,补充研究后重新申报。
申请人名称变更、注册地址名称变更等不涉及技术审评内容的,应当及时书面告知药品审评中心并提交相关证明性资料。
第三节 关联审评审批
第四十一条 药品审评中心在审评药品制剂注册申请时,对药品制剂选用的化学原料药、辅料及直接接触药品的包装材料和容器进行
关联审评。
化学原料药、辅料及直接接触药品的包装材料和容器生产企业应当按照关联审评审批制度要求,在化学原料药、辅料及直接接触药品
的包装材料和容器登记平台登记产品信息和研究资料。药品审评中心向社会公示登记号、产品名称、企业名称、生产地址等基本信息,供
药品制剂注册申请人选择。
第四十二条 药品制剂申请人提出药品注册申请,可以直接选用已登记的化学原料药、辅料及直接接触药品的包装材料和容器;选用
未登记的化学原料药、辅料及直接接触药品的包装材料和容器的,相关研究资料应当随药品制剂注册申请一并申报。
第四十三条 药品审评中心在审评药品制剂注册申请时,对药品制剂选用的化学原料药、辅料及直接接触药品的包装材料和容器进行
关联审评,需补充资料的,按照补充资料程序要求药品制剂申请人或者化学原料药、辅料及直接接触药品的包装材料和容器登记企业补充
资料,可以基于风险提出对化学原料药、辅料及直接接触药品的包装材料和容器企业进行延伸检查。
仿制境内已上市药品所用的化学原料药的,可以申请单独审评审批。
第四十四条 化学原料药、辅料及直接接触药品的包装材料和容器关联审评通过的或者单独审评审批通过的,药品审评中心在化学原
料药、辅料及直接接触药品的包装材料和容器登记平台更新登记状态标识,向社会公示相关信息。其中,化学原料药同时发给化学原料药
批准通知书及核准后的生产工艺、质量标准和标签,化学原料药批准通知书中载明登记号;不予批准的,发给化学原料药不予批准通知
书。
未通过关联审评审批的,化学原料药、辅料及直接接触药品的包装材料和容器产品的登记状态维持不变,相关药品制剂申请不予批
准。
第四节 药品注册核查
第四十五条 药品注册核查,是指为核实申报资料的真实性、一致性以及药品上市商业化生产条件,检查药品研制的合规性、数据可
靠性等,对研制现场和生产现场开展的核查活动,以及必要时对药品注册申请所涉及的化学原料药、辅料及直接接触药品的包装材料和容
器生产企业、供应商或者其他受托机构开展的延伸检查活动。
药品注册核查启动的原则、程序、时限和要求,由药品审评中心制定公布;药品注册核查实施的原则、程序、时限和要求,由药品核
查中心制定公布。
第四十六条 药品审评中心根据药物创新程度、药物研究机构既往接受核查情况等,基于风险决定是否开展药品注册研制现场核查。
药品审评中心决定启动药品注册研制现场核查的,通知药品核查中心在审评期间组织实施核查,同时告知申请人。药品核查中心应当
在规定时限内完成现场核查,并将核查情况、核查结论等相关材料反馈药品审评中心进行综合审评。
第四十七条 药品审评中心根据申报注册的品种、工艺、设施、既往接受核查情况等因素,基于风险决定是否启动药品注册生产现场
核查。
对于创新药、改良型新药以及生物制品等,应当进行药品注册生产现场核查和上市前药品生产质量管理规范检查。
对于仿制药等,根据是否已获得相应生产范围药品生产许可证且已有同剂型品种上市等情况,基于风险进行药品注册生产现场核查、
上市前药品生产质量管理规范检查。
第四十八条 药品注册申请受理后,药品审评中心应当在受理后四十日内进行初步审查,需要药品注册生产现场核查的,通知药品核
查中心组织核查,提供核查所需的相关材料,同时告知申请人以及申请人或者生产企业所在地省、自治区、直辖市药品监督管理部门。药
品核查中心原则上应当在审评时限届满四十日前完成核查工作,并将核查情况、核查结果等相关材料反馈至药品审评中心。
需要上市前药品生产质量管理规范检查的,由药品核查中心协调相关省、自治区、直辖市药品监督管理部门与药品注册生产现场核查
同步实施。上市前药品生产质量管理规范检查的管理要求,按照药品生产监督管理办法的有关规定执行。
申请人应当在规定时限内接受核查。
第四十九条 药品审评中心在审评过程中,发现申报资料真实性存疑或者有明确线索举报等,需要现场检查核实的,应当启动有因检
查,必要时进行抽样检验。
第五十条 申请药品上市许可时,申请人和生产企业应当已取得相应的药品生产许可证。
第五节 药品注册检验
第五十一条 药品注册检验,包括标准复核和样品检验。标准复核,是指对申请人申报药品标准中设定项目的科学性、检验方法的可
行性、质控指标的合理性等进行的实验室评估。样品检验,是指按照申请人申报或者药品审评中心核定的药品质量标准对样品进行的实验
室检验。
药品注册检验启动的原则、程序、时限等要求,由药品审评中心组织制定公布。药品注册申请受理前提出药品注册检验的具体工作程
序和要求以及药品注册检验技术要求和规范,由中检院制定公布。
第五十二条 与国家药品标准收载的同品种药品使用的检验项目和检验方法一致的,可以不进行标准复核,只进行样品检验。其他情
形应当进行标准复核和样品检验。
第五十三条 中检院或者经国家药品监督管理局指定的药品检验机构承担以下药品注册检验:
(一)创新药;
(二)改良型新药(中药除外);
(三)生物制品、放射性药品和按照药品管理的体外诊断试剂;
(四)国家药品监督管理局规定的其他药品。
境外生产药品的药品注册检验由中检院组织口岸药品检验机构实施。
其他药品的注册检验,由申请人或者生产企业所在地省级药品检验机构承担。
第五十四条 申请人完成支持药品上市的药学相关研究,确定质量标准,并完成商业规模生产工艺验证后,可以在药品注册申请受理
前向中检院或者省、自治区、直辖市药品监督管理部门提出药品注册检验;申请人未在药品注册申请受理前提出药品注册检验的,在药品
注册申请受理后四十日内由药品审评中心启动药品注册检验。原则上申请人在药品注册申请受理前只能提出一次药品注册检验,不得同时
向多个药品检验机构提出药品注册检验。
申请人提交的药品注册检验资料应当与药品注册申报资料的相应内容一致,不得在药品注册检验过程中变更药品检验机构、样品和资
料等。
第五十五条 境内生产药品的注册申请,申请人在药品注册申请受理前提出药品注册检验的,向相关省、自治区、直辖市药品监督管
理部门申请抽样,省、自治区、直辖市药品监督管理部门组织进行抽样并封签,由申请人将抽样单、样品、检验所需资料及标准物质等送
至相应药品检验机构。
境外生产药品的注册申请,申请人在药品注册申请受理前提出药品注册检验的,申请人应当按规定要求抽取样品,并将样品、检验所
需资料及标准物质等送至中检院。
第五十六条 境内生产药品的注册申请,药品注册申请受理后需要药品注册检验的,药品审评中心应当在受理后四十日内向药品检验
机构和申请人发出药品注册检验通知。申请人向相关省、自治区、直辖市药品监督管理部门申请抽样,省、自治区、直辖市药品监督管理
部门组织进行抽样并封签,申请人应当在规定时限内将抽样单、样品、检验所需资料及标准物质等送至相应药品检验机构。
境外生产药品的注册申请,药品注册申请受理后需要药品注册检验的,申请人应当按规定要求抽取样品,并将样品、检验所需资料及
标准物质等送至中检院。
第五十七条 药品检验机构应当在五日内对申请人提交的检验用样品及资料等进行审核,作出是否接收的决定,同时告知药品审评中
心。需要补正的,应当一次性告知申请人。
药品检验机构原则上应当在审评时限届满四十日前,将标准复核意见和检验报告反馈至药品审评中心。
第五十八条 在药品审评、核查过程中,发现申报资料真实性存疑或者有明确线索举报,或者认为有必要进行样品检验的,可抽取样
品进行样品检验。
审评过程中,药品审评中心可以基于风险提出质量标准单项复核。
第四章 药品加快上市注册程序
第一节 突破性治疗药物程序
第五十九条 药物临床试验期间,用于防治严重危及生命或者严重影响生存质量的疾病,且尚无有效防治手段或者与现有治疗手段相
比有足够证据表明具有明显临床优势的创新药或者改良型新药等,申请人可以申请适用突破性治疗药物程序。
第六十条 申请适用突破性治疗药物程序的,申请人应当向药品审评中心提出申请。符合条件的,药品审评中心按照程序公示后纳入
突破性治疗药物程序。
第六十一条 对纳入突破性治疗药物程序的药物临床试验,给予以下政策支持:
(一)申请人可以在药物临床试验的关键阶段向药品审评中心提出沟通交流申请,药品审评中心安排审评人员进行沟通交流;
(二)申请人可以将阶段性研究资料提交药品审评中心,药品审评中心基于已有研究资料,对下一步研究方案提出意见或者建议,并
反馈给申请人。
第六十二条 对纳入突破性治疗药物程序的药物临床试验,申请人发现不再符合纳入条件时,应当及时向药品审评中心提出终止突破
性治疗药物程序。药品审评中心发现不再符合纳入条件的,应当及时终止该品种的突破性治疗药物程序,并告知申请人。
第二节 附条件批准程序
第六十三条 药物临床试验期间,符合以下情形的药品,可以申请附条件批准:
(一)治疗严重危及生命且尚无有效治疗手段的疾病的药品,药物临床试验已有数据证实疗效并能预测其临床价值的;
(二)公共卫生方面急需的药品,药物临床试验已有数据显示疗效并能预测其临床价值的;
(三)应对重大突发公共卫生事件急需的疫苗或者国家卫生健康委员会认定急需的其他疫苗,经评估获益大于风险的。
第六十四条 申请附条件批准的,申请人应当就附条件批准上市的条件和上市后继续完成的研究工作等与药品审评中心沟通交流,经
沟通交流确认后提出药品上市许可申请。
经审评,符合附条件批准要求的,在药品注册证书中载明附条件批准药品注册证书的有效期、上市后需要继续完成的研究工作及完成
时限等相关事项。
第六十五条 审评过程中,发现纳入附条件批准程序的药品注册申请不能满足附条件批准条件的,药品审评中心应当终止该品种附条
件批准程序,并告知申请人按照正常程序研究申报。
第六十六条 对附条件批准的药品,持有人应当在药品上市后采取相应的风险管理措施,并在规定期限内按照要求完成药物临床试验
等相关研究,以补充申请方式申报。
对批准疫苗注册申请时提出进一步研究要求的,疫苗持有人应当在规定期限内完成研究。
第六十七条 对附条件批准的药品,持有人逾期未按照要求完成研究或者不能证明其获益大于风险的,国家药品监督管理局应当依法
处理,直至注销药品注册证书。
第三节 优先审评审批程序
第六十八条 药品上市许可申请时,以下具有明显临床价值的药品,可以申请适用优先审评审批程序:
(一)临床急需的短缺药品、防治重大传染病和罕见病等疾病的创新药和改良型新药;
(二)符合儿童生理特征的儿童用药品新品种、剂型和规格;
(三)疾病预防、控制急需的疫苗和创新疫苗;
(四)纳入突破性治疗药物程序的药品;
(五)符合附条件批准的药品;
(六)国家药品监督管理局规定其他优先审评审批的情形。
第六十九条 申请人在提出药品上市许可申请前,应当与药品审评中心沟通交流,经沟通交流确认后,在提出药品上市许可申请的同
时,向药品审评中心提出优先审评审批申请。符合条件的,药品审评中心按照程序公示后纳入优先审评审批程序。
第七十条 对纳入优先审评审批程序的药品上市许可申请,给予以下政策支持:
(一)药品上市许可申请的审评时限为一百三十日;
(二)临床急需的境外已上市境内未上市的罕见病药品,审评时限为七十日;
(三)需要核查、检验和核准药品通用名称的,予以优先安排;
(四)经沟通交流确认后,可以补充提交技术资料。
第七十一条 审评过程中,发现纳入优先审评审批程序的药品注册申请不能满足优先审评审批条件的,药品审评中心应当终止该品种
优先审评审批程序,按照正常审评程序审评,并告知申请人。
第四节 特别审批程序
第七十二条 在发生突发公共卫生事件的威胁时以及突发公共卫生事件发生后,国家药品监督管理局可以依法决定对突发公共卫生事
件应急所需防治药品实行特别审批。
第七十三条 对实施特别审批的药品注册申请,国家药品监督管理局按照统一指挥、早期介入、快速高效、科学审批的原则,组织加
快并同步开展药品注册受理、审评、核查、检验工作。特别审批的情形、程序、时限、要求等按照药品特别审批程序规定执行。
第七十四条 对纳入特别审批程序的药品,可以根据疾病防控的特定需要,限定其在一定期限和范围内使用。
第七十五条 对纳入特别审批程序的药品,发现其不再符合纳入条件的,应当终止该药品的特别审批程序,并告知申请人。
第五章 药品上市后变更和再注册
第一节 药品上市后研究和变更
第七十六条 持有人应当主动开展药品上市后研究,对药品的安全性、有效性和质量可控性进行进一步确证,加强对已上市药品的持
续管理。
药品注册证书及附件要求持有人在药品上市后开展相关研究工作的,持有人应当在规定时限内完成并按照要求提出补充申请、备案或
者报告。
药品批准上市后,持有人应当持续开展药品安全性和有效性研究,根据有关数据及时备案或者提出修订说明书的补充申请,不断更新
完善说明书和标签。药品监督管理部门依职责可以根据药品不良反应监测和药品上市后评价结果等,要求持有人对说明书和标签进行修
订。
第七十七条 药品上市后的变更,按照其对药品安全性、有效性和质量可控性的风险和产生影响的程度,实行分类管理,分为审批类
变更、备案类变更和报告类变更。
持有人应当按照相关规定,参照相关技术指导原则,全面评估、验证变更事项对药品安全性、有效性和质量可控性的影响,进行相应
的研究工作。
药品上市后变更研究的技术指导原则,由药品审评中心制定,并向社会公布。
第七十八条 以下变更,持有人应当以补充申请方式申报,经批准后实施:
(一)药品生产过程中的重大变更;
(二)药品说明书中涉及有效性内容以及增加安全性风险的其他内容的变更;
(三)持有人转让药品上市许可;
(四)国家药品监督管理局规定需要审批的其他变更。
第七十九条 以下变更,持有人应当在变更实施前,报所在地省、自治区、直辖市药品监督管理部门备案:
(一)药品生产过程中的中等变更;
(二)药品包装标签内容的变更;
(三)药品分包装;
(四)国家药品监督管理局规定需要备案的其他变更。
境外生产药品发生上述变更的,应当在变更实施前报药品审评中心备案。
药品分包装备案的程序和要求,由药品审评中心制定发布。
第八十条 以下变更,持有人应当在年度报告中报告:
(一)药品生产过程中的微小变更;
(二)国家药品监督管理局规定需要报告的其他变更。
第八十一条 药品上市后提出的补充申请,需要核查、检验的,参照本办法有关药品注册核查、检验程序进行。
第二节 药品再注册
第八十二条 持有人应当在药品注册证书有效期届满前六个月申请再注册。境内生产药品再注册申请由持有人向其所在地省、自治
区、直辖市药品监督管理部门提出,境外生产药品再注册申请由持有人向药品审评中心提出。
第八十三条 药品再注册申请受理后,省、自治区、直辖市药品监督管理部门或者药品审评中心对持有人开展药品上市后评价和不良
反应监测情况,按照药品批准证明文件和药品监督管理部门要求开展相关工作情况,以及药品批准证明文件载明信息变化情况等进行审
查,符合规定的,予以再注册,发给药品再注册批准通知书。不符合规定的,不予再注册,并报请国家药品监督管理局注销药品注册证
书。
第八十四条 有下列情形之一的,不予再注册:
(一)有效期届满未提出再注册申请的;
(二)药品注册证书有效期内持有人不能履行持续考察药品质量、疗效和不良反应责任的;
(三)未在规定时限内完成药品批准证明文件和药品监督管理部门要求的研究工作且无合理理由的;
(四)经上市后评价,属于疗效不确切、不良反应大或者因其他原因危害人体健康的;
(五)法律、行政法规规定的其他不予再注册情形。
对不予再注册的药品,药品注册证书有效期届满时予以注销。
第六章 受理、撤回申请、审批决定和争议解决
第八十五条 药品监督管理部门收到药品注册申请后进行形式审查,并根据下列情况分别作出是否受理的决定:
(一)申请事项依法不需要取得行政许可的,应当即时作出不予受理的决定,并说明理由。
(二)申请事项依法不属于本部门职权范围的,应当即时作出不予受理的决定,并告知申请人向有关行政机关申请。
(三)申报资料存在可以当场更正的错误的,应当允许申请人当场更正;更正后申请材料齐全、符合法定形式的,应当予以受理。
(四)申报资料不齐全或者不符合法定形式的,应当当场或者在五日内一次告知申请人需要补正的全部内容。按照规定需要在告知时
一并退回申请材料的,应当予以退回。申请人应当在三十日内完成补正资料。申请人无正当理由逾期不予补正的,视为放弃申请,无需作
出不予受理的决定。逾期未告知申请人补正的,自收到申请材料之日起即为受理。
(五)申请事项属于本部门职权范围,申报资料齐全、符合法定形式,或者申请人按照要求提交全部补正资料的,应当受理药品注册
申请。
药品注册申请受理后,需要申请人缴纳费用的,申请人应当按规定缴纳费用。申请人未在规定期限内缴纳费用的,终止药品注册审评
审批。
第八十六条 药品注册申请受理后,有药品安全性新发现的,申请人应当及时报告并补充相关资料。
第八十七条 药品注册申请受理后,需要申请人在原申报资料基础上补充新的技术资料的,药品审评中心原则上提出一次补充资料要
求,列明全部问题后,以书面方式通知申请人在八十日内补充提交资料。申请人应当一次性按要求提交全部补充资料,补充资料时间不计
入药品审评时限。药品审评中心收到申请人全部补充资料后启动审评,审评时限延长三分之一;适用优先审评审批程序的,审评时限延长
四分之一。
不需要申请人补充新的技术资料,仅需要申请人对原申报资料进行解释说明的,药品审评中心通知申请人在五日内按照要求提交相关
解释说明。
药品审评中心认为存在实质性缺陷无法补正的,不再要求申请人补充资料。基于已有申报资料做出不予批准的决定。
第八十八条 药物临床试验申请、药物临床试验期间的补充申请,在审评期间,不得补充新的技术资料;如需要开展新的研究,申请
人可以在撤回后重新提出申请。
第八十九条 药品注册申请受理后,申请人可以提出撤回申请。同意撤回申请的,药品审评中心或者省、自治区、直辖市药品监督管
理部门终止其注册程序,并告知药品注册核查、检验等技术机构。审评、核查和检验过程中发现涉嫌存在隐瞒真实情况或者提供虚假信息
等违法行为的,依法处理,申请人不得撤回药品注册申请。
第九十条 药品注册期间,对于审评结论为不通过的,药品审评中心应当告知申请人不通过的理由,申请人可以在十五日内向药品审
评中心提出异议。药品审评中心结合申请人的异议意见进行综合评估并反馈申请人。
申请人对综合评估结果仍有异议的,药品审评中心应当按照规定,在五十日内组织专家咨询委员会论证,并综合专家论证结果形成最
终的审评结论。
申请人异议和专家论证时间不计入审评时限。
第九十一条 药品注册期间,申请人认为工作人员在药品注册受理、审评、核查、检验、审批等工作中违反规定或者有不规范行为
的,可以向其所在单位或者上级机关投诉举报。
第九十二条 药品注册申请符合法定要求的,予以批准。
药品注册申请有下列情形之一的,不予批准:
(一)药物临床试验申请的研究资料不足以支持开展药物临床试验或者不能保障受试者安全的;
(二)申报资料显示其申请药品安全性、有效性、质量可控性等存在较大缺陷的;
(三)申报资料不能证明药品安全性、有效性、质量可控性,或者经评估认为药品风险大于获益的;
(四)申请人未能在规定时限内补充资料的;
(五)申请人拒绝接受或者无正当理由未在规定时限内接受药品注册核查、检验的;
(六)药品注册过程中认为申报资料不真实,申请人不能证明其真实性的;
(七)药品注册现场核查或者样品检验结果不符合规定的;
(八)法律法规规定的不应当批准的其他情形。
第九十三条 药品注册申请审批结束后,申请人对行政许可决定有异议的,可以依法提起行政复议或者行政诉讼。
第七章 工作时限
第九十四条 本办法所规定的时限是药品注册的受理、审评、核查、检验、审批等工作的最长时间。优先审评审批程序相关工作时
限,按优先审评审批相关规定执行。
药品审评中心等专业技术机构应当明确本单位工作程序和时限,并向社会公布。
第九十五条 药品监督管理部门收到药品注册申请后进行形式审查,应当在五日内作出受理、补正或者不予受理决定。
第九十六条 药品注册审评时限,按照以下规定执行:
(一)药物临床试验申请、药物临床试验期间补充申请的审评审批时限为六十日;
(二)药品上市许可申请审评时限为二百日,其中优先审评审批程序的审评时限为一百三十日,临床急需境外已上市罕见病用药优先
审评审批程序的审评时限为七十日;
(三)单独申报仿制境内已上市化学原料药的审评时限为二百日;
(四)审批类变更的补充申请审评时限为六十日,补充申请合并申报事项的,审评时限为八十日,其中涉及临床试验研究数据审查、
药品注册核查检验的审评时限为二百日;
(五)药品通用名称核准时限为三十日;
(六)非处方药适宜性审核时限为三十日。
关联审评时限与其关联药品制剂的审评时限一致。
第九十七条 药品注册核查时限,按照以下规定执行:
(一)药品审评中心应当在药品注册申请受理后四十日内通知药品核查中心启动核查,并同时通知申请人;
(二)药品核查中心原则上在审评时限届满四十日前完成药品注册生产现场核查,并将核查情况、核查结果等相关材料反馈至药品审
评中心。
第九十八条 药品注册检验时限,按照以下规定执行:
(一)样品检验时限为六十日,样品检验和标准复核同时进行的时限为九十日;
(二)药品注册检验过程中补充资料时限为三十日;
(三)药品检验机构原则上在审评时限届满四十日前完成药品注册检验相关工作,并将药品标准复核意见和检验报告反馈至药品审评
中心。
第九十九条 药品再注册审查审批时限为一百二十日。
第一百条 行政审批决定应当在二十日内作出。
第一百零一条 药品监督管理部门应当自作出药品注册审批决定之日起十日内颁发、送达有关行政许可证件。
第一百零二条 因品种特性及审评、核查、检验等工作遇到特殊情况确需延长时限的,延长的时限不得超过原时限的二分之一,经药
品审评、核查、检验等相关技术机构负责人批准后,由延长时限的技术机构书面告知申请人,并通知其他相关技术机构。
第一百零三条 以下时间不计入相关工作时限:
(一)申请人补充资料、核查后整改以及按要求核对生产工艺、质量标准和说明书等所占用的时间;
(二)因申请人原因延迟核查、检验、召开专家咨询会等的时间;
(三)根据法律法规的规定中止审评审批程序的,中止审评审批程序期间所占用的时间;
(四)启动境外核查的,境外核查所占用的时间。
第八章 监督管理
第一百零四条 国家药品监督管理局负责对药品审评中心等相关专业技术机构及省、自治区、直辖市药品监督管理部门承担药品注册
管理相关工作的监督管理、考核评价与指导。
第一百零五条 药品监督管理部门应当依照法律、法规的规定对药品研制活动进行监督检查,必要时可以对为药品研制提供产品或者
服务的单位和个人进行延伸检查,有关单位和个人应当予以配合,不得拒绝和隐瞒。
第一百零六条 信息中心负责建立药品品种档案,对药品实行编码管理,汇集药品注册申报、临床试验期间安全性相关报告、审评、
核查、检验、审批以及药品上市后变更的审批、备案、报告等信息,并持续更新。药品品种档案和编码管理的相关制度,由信息中心制定
公布。
第一百零七条 省、自治区、直辖市药品监督管理部门应当组织对辖区内药物非临床安全性评价研究机构、药物临床试验机构等遵守
药物非临床研究质量管理规范、药物临床试验质量管理规范等情况进行日常监督检查,监督其持续符合法定要求。国家药品监督管理局根
据需要进行药物非临床安全性评价研究机构、药物临床试验机构等研究机构的监督检查。
第一百零八条 国家药品监督管理局建立药品安全信用管理制度,药品核查中心负责建立药物非临床安全性评价研究机构、药物临床
试验机构药品安全信用档案,记录许可颁发、日常监督检查结果、违法行为查处等情况,依法向社会公布并及时更新。药品监督管理部门
对有不良信用记录的,增加监督检查频次,并可以按照国家规定实施联合惩戒。药物非临床安全性评价研究机构、药物临床试验机构药品
安全信用档案的相关制度,由药品核查中心制定公布。
第一百零九条 国家药品监督管理局依法向社会公布药品注册审批事项清单及法律依据、审批要求和办理时限,向申请人公开药品注
册进度,向社会公开批准上市药品的审评结论和依据以及监督检查发现的违法违规行为,接受社会监督。
批准上市药品的说明书应当向社会公开并及时更新。其中,疫苗还应当公开标签内容并及时更新。
未经申请人同意,药品监督管理部门、专业技术机构及其工作人员、参与专家评审等的人员不得披露申请人提交的商业秘密、未披露
信息或者保密商务信息,法律另有规定或者涉及国家安全、重大社会公共利益的除外。
第一百一十条 具有下列情形之一的,由国家药品监督管理局注销药品注册证书,并予以公布:
(一)持有人自行提出注销药品注册证书的;
(二)按照本办法规定不予再注册的;
(三)持有人药品注册证书、药品生产许可证等行政许可被依法吊销或者撤销的;
(四)按照《药品管理法》第八十三条的规定,疗效不确切、不良反应大或者因其他原因危害人体健康的;
(五)按照《疫苗管理法》第六十一条的规定,经上市后评价,预防接种异常反应严重或者其他原因危害人体健康的;
(六)按照《疫苗管理法》第六十二条的规定,经上市后评价发现该疫苗品种的产品设计、生产工艺、安全性、有效性或者质量可控
性明显劣于预防、控制同种疾病的其他疫苗品种的;
(七)违反法律、行政法规规定,未按照药品批准证明文件要求或者药品监督管理部门要求在规定时限内完成相应研究工作且无合理
理由的;
(八)其他依法应当注销药品注册证书的情形。
第九章 法律责任
第一百一十一条 在药品注册过程中,提供虚假的证明、数据、资料、样品或者采取其他手段骗取临床试验许可或者药品注册等许可
的,按照《药品管理法》第一百二十三条处理。
第一百一十二条 申请疫苗临床试验、注册提供虚假数据、资料、样品或者有其他欺骗行为的,按照《疫苗管理法》第八十一条进行
处理。
第一百一十三条 在药品注册过程中,药物非临床安全性评价研究机构、药物临床试验机构等,未按照规定遵守药物非临床研究质量
管理规范、药物临床试验质量管理规范等的,按照《药品管理法》第一百二十六条处理。
第一百一十四条 未经批准开展药物临床试验的,按照《药品管理法》第一百二十五条处理;开展生物等效性试验未备案的,按照
《药品管理法》第一百二十七条处理。
第一百一十五条 药物临床试验期间,发现存在安全性问题或者其他风险,临床试验申办者未及时调整临床试验方案、暂停或者终止
临床试验,或者未向国家药品监督管理局报告的,按照《药品管理法》第一百二十七条处理。
第一百一十六条 违反本办法第二十八条、第三十三条规定,申办者有下列情形之一的,责令限期改正;逾期不改正的,处一万元以
上三万元以下罚款:
(一)开展药物临床试验前未按规定在药物临床试验登记与信息公示平台进行登记;
(二)未按规定提交研发期间安全性更新报告;
(三)药物临床试验结束后未登记临床试验结果等信息。
第一百一十七条 药品检验机构在承担药品注册所需要的检验工作时,出具虚假检验报告的,按照《药品管理法》第一百三十八条处
理。
第一百一十八条 对不符合条件而批准进行药物临床试验、不符合条件的药品颁发药品注册证书的,按照《药品管理法》第一百四十
七条处理。
第一百一十九条 药品监督管理部门及其工作人员在药品注册管理过程中有违法违规行为的,按照相关法律法规处理。
第十章 附 则
第一百二十条 麻醉药品、精神药品、医疗用毒性药品、放射性药品、药品类易制毒化学品等有其他特殊管理规定药品的注册申请,
除按照本办法的规定办理外,还应当符合国家的其他有关规定。
第一百二十一条 出口疫苗的标准应当符合进口国(地区)的标准或者合同要求。
第一百二十二条 拟申报注册的药械组合产品,已有同类产品经属性界定为药品的,按照药品进行申报;尚未经属性界定的,申请人
应当在申报注册前向国家药品监督管理局申请产品属性界定。属性界定为药品为主的,按照本办法规定的程序进行注册,其中属于医疗器
械部分的研究资料由国家药品监督管理局医疗器械技术审评中心作出审评结论后,转交药品审评中心进行综合审评。
第一百二十三条 境内生产药品批准文号格式为:国药准字H(Z、S)+四位年号+四位顺序号。中国香港、澳门和台湾地区生产药
品批准文号格式为:国药准字H(Z、S)C+四位年号+四位顺序号。
境外生产药品批准文号格式为:国药准字H(Z、S)J+四位年号+四位顺序号。
其中,H代表化学药,Z代表中药,S代表生物制品。
药品批准文号,不因上市后的注册事项的变更而改变。
中药另有规定的从其规定。
第一百二十四条 药品监督管理部门制作的药品注册批准证明电子文件及原料药批准文件电子文件与纸质文件具有同等法律效力。
第一百二十五条 本办法规定的期限以工作日计算。
第一百二十六条 本办法自2020年7月1日起施行。2007年7月10日原国家食品药品监督管理局令第28号公布的《药品注册管理办
法》同时废止。
为鼓励新药研发,在国家药品监督管理局的部署下,药审中心组织制定了《西妥昔单抗注射液生物类似药临床试验设计指导原则(试
行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品
监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年1月17日
根据国家局2019年3月28日发布的《关于发布化学仿制药参比制剂遴选与确定程序的公告》(2019年第25号),我中心组织遴选了第
五十七批参比制剂(见附件),现予以公示征求意见。
公示期间,请通过参比制剂遴选申请平台下“参比制剂存疑品种申请”模块向药审中心进行反馈,为更好服务申请人,反馈意见请提供
充分依据和论证材料,反馈材料应加盖单位公章,并提供真实姓名和联系方式。
公示期限:2022年3月25日~2022年4月8日(10个工作日)。
国家药品监督管理局药品审评中心
2022年3月25日
为进一步鼓励和促进儿童用药的研制和创新,由国家药品监督管理局药品审评中心和中国药品监督管理研究会联合主办的“儿童用药相
关指导原则宣讲会”于2022年3月1日和8日以线上直播方式举办。这两次宣讲会分专业围绕学界和业界具有较高关注度的儿童用药指导原则
进行了介绍和解读,加强了与临床机构、研发企业的沟通交流。
现将两场宣讲会的课件资料在网站发布,供观看学习。
附件:儿童用药指导原则宣讲会课件资料
国家药品监督管理局药品审评中心
2022年3月21日
为鼓励研发儿童用药,交流儿童用药研发中的新技术、新方法,我中心组织开展“儿童用药口感设计与评价专题研讨会”,现将相关事
宜通知如下:
一、培训时间
2022年3月24日(周四),上午09:00 - 11:00
二、培训形式
视频培训
三、主讲人及培训内容
序号 | 姓名 | 单位名称 | 培训内容 |
1 | 王晓玲 | 国家儿童医学中心(首都医科大学附属北京儿童医院) | 儿童用药口感设计与评价的价值与需求 |
2 | 彭晓霞 | 国家儿童医学中心(首都医科大学附属北京儿童医院) | 儿童用药口感设计与评价的研究方法学进展 |
3 | 王坚成 | 北京大学药学院 | 儿童用药口感设计与评价药学技术难点及研发策略分析 |
四、参会要求
请有意向参会者填写附件报名表,并于2022年3月21日17:00前发至邮箱地址:etdrugs@cde.org.cn。本次会议规模200人,根据收
到邮件的先后顺序确定参会名额。
药品审评中心
2022年3月15日
化学药品改良型新药临床试验技术指导原则》自2020年12月正式发布以来,改良型新药临床研发的沟通交流逐渐增多,为进一步促进
我国改良型新药有序研发,更好满足患者的临床需求,指导原则工作组经过系统梳理,就比较集中的共性问题进行讨论,形成了《<化学药
品改良型新药临床试验技术指导原则>问与答(征求意见稿)》。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起一个
月。
您的反馈意见请发到以下联系人的邮箱:
联系人:宋媛媛, 艾星
联系方式:songyy@cde.org.cn, aix@cde.org.cn,
感谢您的参与和大力支持。
国家药品监督管理局药品审评中心
2022年3月14日
编号:Fg2022-0049号
我委拟修订聚乙烯醇药用辅料标准,为确保标准的科学性、合理性和适用性,现将拟制定(修订)的药用辅料标准公示征求社会
各界意见(详见附件)。公示期自发布之日起3个月。请认真研核,若有异议,请及时来函提交反馈意见,并附相关说明、实验数据
和联系方式。相关单位来函需加盖公章,个人来函需本人签名,同时将电子版发送至指定邮箱。
联系人:陈蕾、康笑博
电话:010-67079566、67079620
电子邮箱:475@chp.org.cn
通信地址:北京市东城区法华南里11号楼 国家药典委员会办公室
邮编:100061
国家药典委员会
2022年03月11日
联系人:陈蕾、康笑博
电话:010-67079566、67079620
电子邮箱:475@chp.org.cn
通信地址:北京市东城区法华南里11号楼 国家药典委员会办公室
邮编:100061
国家药典委员会
2022年03月11日
药物上市的根本目的是解决患者的需求。药物研发应以患者需求为核心,以临床价值为导向已经成为普遍共识。目前我国抗肿瘤药物研
发处于快速发展阶段;肿瘤患者对于药物的安全性、治疗体验和生存质量都有了更高的期望。抗肿瘤药物研发,从确定研 发方向,到开展临
床试验,都应贯彻以临床需求为核心的理念,开展以临床价值为导向的抗肿瘤药物研发。
为落实以临床价值为导向,以患者需求为核心的研发理念,促进抗肿瘤药科学有序的开发,药品审评中心组织撰写了《以临床价值为导
向的抗肿瘤药物临床研发指导原则》,形成征求意见稿。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个月。
您的反馈意见请发到以下联系人的邮箱;
为鼓励新药研发,在国家药品监督管理局的部署下,药审中心组织制定了《长效重组人粒细胞集落刺激因子预防化疗后中性粒细胞减少
性发热临床试验设计指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管
〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
附件:长效重组人粒细胞集落刺激因子预防化疗后中性粒细胞减少性发热临床试验设计指导原则(试行)
国家药监局药审中心
2022年1月17日
根据国家局2019年3月28日发布的《关于发布化学仿制药参比制剂遴选与确定程序的公告》(2019年第25号),我中心组织遴选了第
五十六批参比制剂(见附件),现予以公示征求意见。
公示期间,请通过参比制剂遴选申请平台下“参比制剂存疑品种申请”模块向药审中心进行反馈,为更好服务申请人,反馈意见请提
供充分依据和论证材料,反馈材料应加盖单位公章,并提供真实姓名和联系方式。
公示期限:2022年3月1日~2022年3月14日(10个工作日)。
国家药品监督管理局药品审评中心
2022年3月1日
为指导和规范人用狂犬病疫苗临床试验,提供可参考的技术规范,在国家药品监督管理局的部署下,药审中心组织制定了《人用狂犬病
疫苗临床研究技术指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管
〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年2月18日
为指导和规范人纤维蛋白原用于先天性纤维蛋白原缺乏症和获得性纤维蛋白原缺乏症的临床试验,在国家药品监督管理局的部署下,药
审中心组织制定了《人纤维蛋白原临床试验技术指导原则(试行)》
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同
意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年2月17日
为指导化药口服固体制剂混合均匀度和中控剂量单位均匀度的研究,提供可参考的技术标准,在国家药品监督管理局的部署下,药审中
心组织制定了《化药口服固体制剂混合均匀度和中控剂量单位均匀度研究技术指导原则(试行)》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年2月8日
为指导新型冠状病毒肺炎抗病毒药物的科学研发和评价,提供可供参考的技术标准,药审中心制定了《新型冠状病毒肺炎抗病毒新药临
床试验技术指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕
9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
附件:新型冠状病毒肺炎抗病毒新药临床试验技术指导原则(试行)
国家药监局药审中心
2022年2月8日
为鼓励研究和创制新药,满足临床用药需求,及时总结转化抗疫应急审评工作经验,加快创新药品的审评速度,药审中心组织起草了
《药审中心加快创新药上市申请审评工作程序(试行)》,现在中心网站予以公示,广泛听取社会各界意见和建议。欢迎社会各界提出宝贵
意见和建议,并请通过以下邮箱及时反馈我中心。
征求意见时限:自公示之日起两周。
联系人:张帆、邸云瑞
征求意见邮箱:jkss@cde.org.cn
感谢您的参与和大力支持。
附件:1.《药审中心加快创新药上市申请审评工作程序(试行)》(征求意见稿)
2.《药审中心加快创新药上市申请审评工作程序(试行)》起草说明
3.意见反馈表
国家药品监督管理局药品审评中心
2022年2月21日
原国家食品药品监督管理总局于 2016 年 3 月发布了《以药动学参数为终点评价指标的化学药物仿制药人体生物等效性研究技术指导
原则》,该指导原则提出:对于多规格口服固体制剂(如,常释制剂:片剂和胶囊,调释制剂:肠溶片、缓释片剂、缓释胶囊等),可以
基于其中某一规格(通常建议为最高规格)的人体生物等效性试验结果,采用体外药学评价的方法豁免其他规格人体生物等效性研究。药
学评价方法包括:1)各规格制剂在不同 pH 介质中体外溶出曲线相似;2)各规格制剂的处方比例相似。其中处方比例相似是指以下两种
情况: 1)不同规格之间所有活性和非活性组分组成比例相似。2)对于高活性的药物(原料药在制剂中所占重量比例低):①不同规格
的制剂重量一致(差异不超过10%);②各规格使用相同的非活性组分;③规格的变更系通过改变活性组分的用量以及一个或多个非活性
组分的用量来实现。为更好的指导企业进行仿制药的开发,降低研发成本,提高研发效率,现对该指导原则中的“处方比例相似性”的相
关问题进行解读。
一、“不同规格”、“各规格”的具体所指?
答:“不同规格”、“各规格”是指仿制药拟豁免规格与仿制药 BE 规格相比。
二、“组成比例相似”如何理解?
答:对于常释制剂:“组成比例相似”包括以下情况:①不同规格之间所有非活性和活性组分组成比例完全相同;②不同规格之间所
有非活性成分和活性成份比例基本相同,即在处方等比放大或缩小的基础上,不同规格之间非活性成分的变化幅度在《已上市化学药品变
更研究的技术指导原则(试行)》辅料用量变更中的普通口服固体制剂中等变更允许的范围内;③不同规格之间非活性成分和活性成分的比
例不相似,如申请人申请豁免,应提供可视为处方相似的充分理由,监管机构在审评期间进行综合评估。[8]
对于调释制剂:“组成比例相似”包括以下情况:①不同规格之间所有非活性成分与活性成份的比例完全相同;②不同规格之间非活
性成分与活性成分的比例不完全相同,如申请人申请豁免,应证明比例是合理的,且与产品的药物释放机制相适应。审评期间基于整体资
料进行综合评估。[8]
三、“高活性药物”如何判断? “高活性药物”是活性成分的含量在制剂中相对较低的药物,如,活性成分的含量在片芯和胶囊内容
物的占比<5%[1,3]。
四、不同规格之间非活性成分的变化幅度如何计算?
答:非活性组分是除活性成分外的其它成分[1,2],当不同规格活性成分和非活性成分非等比例变化时,先计算不同规格的非活性成
分相对于单剂量处方的比例,后计算不同规格间的差值[3,4,5]。当处方中非活性变化种类多于一种时,非活性成分的变化幅度应为各
非活性成分变化量的绝对值之和。
五、具体实例
(一)例 1:常释片剂 1
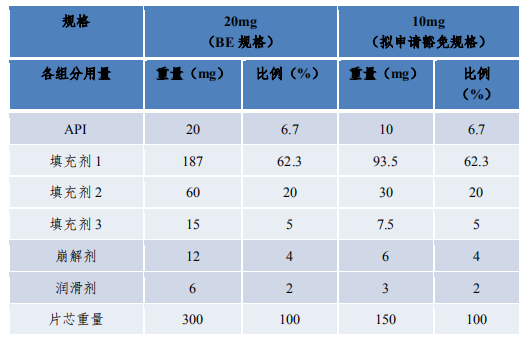
例1中 20mg 规格为 BE 规格。拟申请豁免的 10mg 规格与 BE 规格的所有活性和非活性组分组成比例完全相同,属于常释制剂“不
同规格之间所有活性和非活性组分组成比例完全相同”,结合 BE 规格制剂符合生物等效性要求,且两个规格仿制药在不同 pH 介质中体
外溶出曲线相似的前提条件,可以豁免 10mg 规格的 BE 试验。
(二)例 2:常释片剂 2
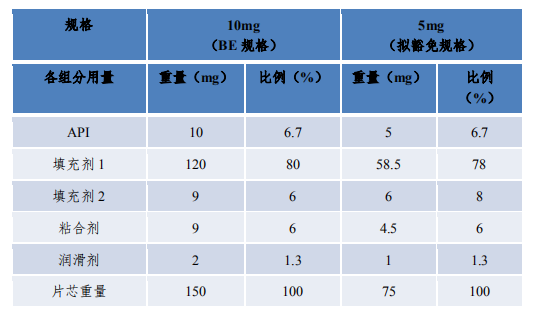
例 2 中 10mg 规格为 BE 规格。拟申请豁免 5mg 规格在BE 规格处方等比缩小的基础上,调整了填充剂 1、填充剂 2的用量。按问题
4 计算方式,计算 5mg 规格与 BE 规格的填充剂 1 变化幅度 80%-78%=2%,填充剂 2 变化幅度 8%-6%=2%,填充剂总变化幅4%,
小于《已上市化学药品药学变更研究技术指导原则》(试行)辅料用量变更中的Ⅱ类变更允许的范围(±10%)内,故 5mg 规格属于常
释制剂“不同规格之间所有非活性成分和活性成份比例基本相同”的情形。结合 BE 规格制剂符合生物等效性要求,且各规格仿制药在不
同 pH 介质中体外溶出曲线相似的前提条件,可以豁免 BE 试验。
(三)例 3:缓释制剂
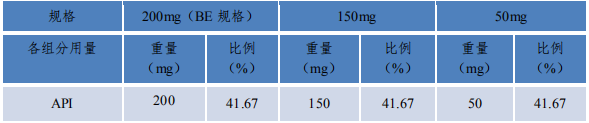
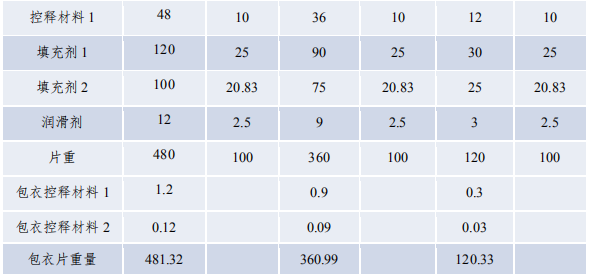
例 3 中 200mg 规格为 BE 规格。拟申请豁免 50mg、150mg 规格与 BE 规格的所有活性和非活性组分组成比例完全相同,属于调释
制剂“不同规格之间所有活性和非活性组分组成比例完全相同”,结合 BE 规格制剂符合生物等效性要求,两个规格制剂与 BE 制剂释药
原理相同,且两个规格与 BE 规格仿制药在三种 pH 介质中体外溶出曲线相似的前提条件,可以豁免 50mg、150mg 规格的 BE 试验。
(四)例 4:普通片剂 3(高活性药物)
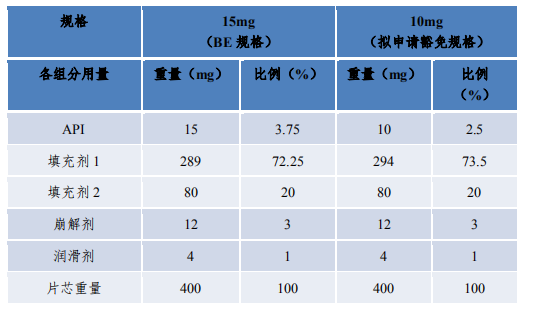
例 4 中 15mg 规格为 BE 规格。拟申请豁免的 10mg 规格与 BE 规格相比,原料药在制剂中所占重量比例均小于5%,属于高活性药
物。不同规格的制剂重量一致,各规格使用相同的非活性组分,规格的变更系通过改变活性组分的用量以及填充剂用量实现的。结合 BE
规格制剂符合生物等效性要求,且各规格仿制药在不同 pH 介质中体外溶出曲线相似的前提条件,可以豁免 10mg 规格的 BE 试验。
参考文献:
1 、 Guidance on the Investigation of Bioequivalence.European Medicines Agency. Janunary 2010.
2 、 §320.22 Criteria for waiver of evidence of in vivo bioavailability or bioequivalence.
3、Bioavailability Studies Submitted in NDAs or INDs —General Considerations Guidance for Industry(Draft Guidance).
FDA February 2019.
4、SUPAC-IR: Immediate-Release Solid Oral Dosage Forms: Scale-Up and Post-Approval Changes: Chemistry, Manufacturing
and Controls, In Vitro Dissolution Testing, and In Vivo Bioequivalence Documentation (I) 11/30/1995
5、SUPAC-MR: Modified Release Solid Oral Dosage Forms: Scale-Up and Postapproval Changes: Chemistry, Manufacturing,
and Controls, In Vitro Dissolution Testing, and In Vivo Bioequivalence Documentation (I) 10/6/1997
6、Bioequivalence Studies with Pharmacokinetic Endpoints for Drugs Submitted Under an ANDA(Draft Guidance). FDA
December 2013.
7、Guidance for Industry:Bioavailability and Bioequivalence Studies Submitted in NDAs or INDs —General Considerations
(Draft Guidance). FDA March 2014.
8、《已上市化学药品变更研究的技术指导原则(试行)》2021 年 2 月 9、Bioequivalence Studies With Pharmacokinetic Endpoints
for Drugs Submitted Under an ANDA Guidance for Industry(Draft Guidance). FDA August 2021.
近年来,生物类似药的研发和申报日益增多。为规范生物类似药的研发和评价,进一步指导生物类似药临床药理学研究,药审中心组织
制定了《生物类似药临床药理学研究技术指导原则》(见附件)。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年2月8日
一、概述
目前中国已经颁布了《2014版中国麻醉学指南与专家共识》和《2017版中国麻醉学指南与专家共识》,后续还没有新的指南和共识
颁布。两版指南在肌松药和肌松拮抗剂的使用场景、药品种类和给与方法上基本一致。但是2017年的指南中对深度肌松单独进行了阐述,
对深肌松的目的和方法进行了详细的介绍,对肌松残留阻滞预防作了更详细的描述,以下就2017版指南与与共识中深肌松和肌松残留阻滞
预防进行探讨。
二、《2017版中国麻醉学指南与专家共识》对深肌松的描述
1、目的:
(1)腹腔镜手术时既能提供良好的窥视和操作空间,同时能降低气腹压,减少不良反应。
(2)避免颅内、喉部、中耳或眼部等精细手术时患者发生不自主的运动。
(3)避免纤维支气管镜下取肺组织活检时患者意外发生呛咳。
(4)避免精神病患者行电抽搐治疗时发生组织损伤。
2、方法
麻醉诱导时静脉注射2倍ED95罗库溴铵或顺阿曲库铵能换得持续约30min深度肌松(PCT1-2),3倍ED95能获得持续约50min深度
肌松,此后每30min静脉注射罗库溴铵0.2mg/kg能维持深度肌松;静脉麻醉维持深度肌松时,持续静脉输注罗库溴铵的初始速率为
3-4mg/(kg.h),在PTC监测下逐步调整至维持深度肌松的适宜速率。手术结束时静脉注射舒更葡糖钠(布瑞亭)4mg/kg后3-5min,
TOF(T4/T1)恢复到0.9以上,能快速逆转罗库溴铵深度阻滞作用,使神经肌肉传导功能恢复正常。如以17μg/(kg.min)的速率持续输
注米库氯铵亦能维持深度肌松,术毕TOFr自然恢复到0.75约10-15min,神经肌肉传导功能也能够较快恢复。肌松药量效反应存在明显个
体差异,弱通过肌松药获得深度肌松,应加强肌松深度的密切监测,从而能及时调整肌松药剂量或输注速率,获得稳定的深度阻滞。
三、《2017版中国麻醉学指南与专家共识》中关于肌松药残留阻滞作用的防治
尽管临床上已广泛应用中短效肌松药,并对其药理作用的认识逐步深化,但术后肌松残留阻滞作用仍时有发生。2015年我国多中心调
查研究结果显示,各类全麻手术结束拔除气管内导管时的肌松残留发生率为36%,而全麻腹部手术结束拔除气管内导管时肌松残留发生率
高达57%,肌松残留严重者可危及生命。
1、肌松残留阻滞作用的危害
(1)呼吸肌无力,肺泡有效通气量不足,导致低氧血症和高碳酸血症。
(2)舌和咽喉部肌无力,不能维持上呼吸道通畅;分泌物集聚,吞咽肌群协调功能未完全恢复正常,易导致上呼吸道梗阻,增加反流误
吸的风险。
(3)咳嗽无力,无法有效排除呼吸道内分泌物,引起术后肺部并发症。
(4)颈动脉体却养性通气反应受抑制,导致低氧血症。
(5)患者术后出现乏力,复视等不适征象。
2、肌松药残留阻滞作用的原因
(1)未能够根据患者病情特点和手术需求合理选用肌松药。
(2)长时间或多次应用中长时效非去极化肌松药。
(3)复合应用与肌松药有协同作用的药物。
(4)个体差异:老龄、女性、肌肉不发达和慢性消耗患者肌松药作用时间延长、
(5)低体温,水电解质紊乱及酸碱失衡,延长肌松药的代谢和排出,乙酰胆碱的合成和神经末梢乙酰胆碱囊泡释放受损。
(6)肝肾功能严重受损,导致体内肌松药代谢,清除障碍。
(7)神经肌肉疾病。
3、肌松药残留阻滞作用的评估
(1)肌松监测仪能够及时,客观和定量地了解肌松药是否存在残留阻滞作用。
早期认为TOFr>0.7时肌松药的残留作用已经消除,但进一步研究证实呼吸肌对肌松药较不敏感,呼吸肌从肌松作用中回复较早,当
TOFr>0.7时,呼吸功能已经基本回复,但咽喉部肌肉肌力恢复较晚,在TOFr≥0.9咽喉部肌肉的协调功能才能够不受损害。因此,
TOFr<0.9提示存在肌松药残留阻滞作用。
(2)无肌松残留的临床指征
①意识清醒,呛咳和吞咽反射恢复;
②头能持续抬离枕头5s以上(反映肌肉强直收缩力);
③呼吸平稳,呼吸频率10-20/min,最大吸气压≤-50cmH2O;
④PetCO2和PaCO2≤45mmHg。
上述4项为肌松药残留阻滞作用基本消除较为可靠的临床指征。
4、肌松药残留阻滞作用的预防
(1)根据患者情况和手术需要,选用合适的肌松药和剂量,应给与能满足手术要求的最低剂量。
(2)改善患者全身情况,维持电解质和酸碱平衡正常。
(3)术毕无明确指征显示肌松药残留阻滞作用已完全消退,应进行肌松药残留阻滞作用的拮抗。
(4)拔除气管内导管后,应在手术室或恢复室严密观测患者神志、保护性反射,呼吸道通畅度,肺泡通气量及氧合状态至少30min,
确保患者安全。
(5)监测肌力恢复情况,注意肌松药药效的个例差异。
5、非去极化肌松药残留阻滞作用的拮抗
(1)胆碱酯酶抑制剂:胆碱酯酶抑制剂新斯的明可抑制乙酰胆碱酯酶,增加神经肌肉接头部乙酰胆碱的浓度,竞争性拮抗非去极化肌
松药的残留阻滞作用;但同时会出现肠蠕动增强,分泌物增多,支气管痉挛和心率减慢等毒覃碱样胆碱能受体兴奋的不良反应,因此需同
时应用抗胆碱药。给与新斯的明时首选格隆溴铵,在我国常用阿托品。胆碱酯酶抑制剂拮抗残留肌松作用的效果与其剂量和拮抗时机密切
相关。
①拮抗时机:通常给与中时效肌松药后30min以上,长时效肌松药1h以上,TOF计数≥2或开始有自住呼吸时拮抗剂送药残留阻滞作用。
②拮抗药剂量:新斯的明0.04-0.07mg/kg,最大剂量5mg,起效时间2min,达峰时间7-1min,作用持续时间2h。若用量偏小,则难
以达到满意的拮抗效果,肌力恢复不完全,;但新斯的明的拮抗作用有封顶效应,不能无限增加其剂量,如果已经达最大剂量,再追加时,
既不能进一步拮抗非去极化肌松药残留作用,还会出现大剂量新斯的明的肌松效应以及可能出现胆碱能危象(睫状肌痉挛、心律失常、冠状
动脉痉挛)。因此已经给予最大剂量新斯的明后,若患者呼吸仍不能够满足要求,应进行有效的人工通气,认真分析影响肌松药拮抗效果
的原因,采取相应的措施,阿托品和新斯的明用同一注射器缓慢静脉注射,阿托品的剂量一般为新斯的明的半量或三分之一。需跟进患者
心率调整阿托品的剂量。静脉注射阿托品后10-30s起效,达峰时间12-16min,作用持续时间为4-6h,故给予拮抗药后患者心率通常会增快。
③拮抗药使用注意事项
A、下列情况禁用或慎用新斯的明:支气管哮喘,心率失常,尤其是房室传导阻滞,心肌缺血,瓣膜严重狭窄;机械性肠根阻;尿路感
染或尿路梗阻;妊娠妇女;对溴化物过敏等;
B、下列情况禁用或慎用阿托品:痉挛性麻痹与脑损伤的小儿;心率失常,充血性心力衰竭,冠心病,二尖瓣狭窄;反流性食管炎;食
管与胃的运动减弱;青光眼;溃疡性结肠炎;前列腺肥大及尿路阻塞性疾病等;
C、电解质异常和酸碱失衡、肾衰竭、高龄和同时接受肌松协同作用药物患者,新斯的明对肌松药残留阻滞作用的拮抗效果并不理想;
D、给与胆碱酯酶抑制剂拮抗残留肌松作用后,需严密监测患者的肌力恢复情况,严防出现再箭毒化,特别是接受长时效或大剂量肌松
药时;
E、凡禁用胆碱酯酶抑制剂或抗胆碱药者,可选用甾类肌松药特异性拮抗剂(布瑞亭),在肌力未充分恢复之前应进行有效人工通气。
(2)布瑞亭(舒更葡糖钠)
布瑞亭是新型氨基甾类肌松药特异性拮抗剂,为修饰后的γ-环糊精。其以一个分子对一个分子的形式选择性,高亲和性地包裹罗库溴
铵或维库溴铵后,经肾脏排出,从而使血液和组织中的罗库溴铵或维库溴铵的浓度急剧下降,神经肌肉接头功能恢复常态。麻醉诱导后立
即逆转罗库溴铵极深阻滞时(PTC=0),需静脉注射布瑞亭16mg/kg;当罗库溴铵达到深度阻滞时(PTC=1-2),静脉注射布瑞亭
4mg/kg可立即终止罗库溴铵作用;当TOF监测T2再现时静脉注射布瑞亭2mg/kg,2min内TOFr可恢复到0.9;当TOFr=0.5时静脉注射布
瑞亭0.2mg/kg,亦可在2min内消除罗库溴铵残留阻滞作用。给与布瑞亭不需要伍用抗胆碱药,避免抗胆碱药可能引起的不良反应。国外
大量数据表明,在成人,儿童、老年以及肾衰竭、肺部或心脏疾病患者中,布瑞亭耐受性良好。布瑞亭对苄异喹啉类肌松药无拮抗作用,
如果给与布瑞亭后手术意外需要进行肌肉松弛,可使用苄异喹啉类肌松药。临床应用布瑞亭能够明显降低术后肌松药残留阻滞作用的发生
率,显著提高罗库溴铵和维库溴铵临床应用的安全性,同时也明显提高麻醉质量。
三、《2017版中国麻醉学指南与专家共识》对Aom0498临床应用的影响
从2017年颁布的指南中可以看出,对临床上深肌松应用进行了详细的指导,由于深肌松中肌松药的使用量较大,因此推荐同时使用肌
松拮抗剂布瑞亭,对患者的恢复可起到积极的作用,推荐手术结束时静脉注射舒更葡糖钠(布瑞亭)4mg/kg后3-5min,TOF(T4/T1)
恢复到0.9以上,能快速逆转罗库溴铵深度阻滞作用,使神经肌肉传导功能恢复正常。而其他胆碱酯酶抑制剂对深肌松无拮抗作用,因此深
肌松时必须使用布瑞亭,Aom0498与布瑞亭作用机制相同,因此在后续的临床使用中,也会得到相应的推广使用。
另外,2017版指南与共识也强调了肌松残留的危害,并提出在临床上已逐渐被认知,2015年我国多中心调查研究结果显示,各类全麻
手术结束拔除气管内导管时的肌松残留发生率为36%,而全麻腹部手术结束拔除气管内导管时肌松残留发生率高达57%,肌松残留严重者
可危及生命。因此,采用肌松拮抗剂在手术中的必要性越来越被临床医生认可并应用。
最后,传统的胆碱酯酶抑制剂新斯的明副作用较大,常需要伍用抗胆碱药物阿托品,且存在较多禁忌的情况,临床上再箭毒化发生率比
布瑞亭高,且不能拮抗深度肌松,在行深肌松的腹腔镜手术,肺组织活检手术,颅内、喉部、中耳或眼部等精细手术中发生肌松残留的情况
较大,而传统的肌松拮抗剂达不到理想的效果,布瑞亭可以再3-5min逆转肌松作用,使患者的恢复更快,更好,而且在胆碱酯酶抑制剂禁
忌的情况下均可选择布瑞亭作用肌松拮抗药物。随着指南和共识中对手术中深肌松的应用和重视,及对布瑞亭的推荐使用,相信对后续
Aom0498的临床应用和推广都将起到积极正面的作用。
附表:肌松拮抗剂的研发进展
| 时间 | 肌松拮抗剂 | 临床使用情况 |
2008年以前 | 去极化肌松药(琥珀胆碱)的残留阻滞拮抗:至今没有有效药物,多采用机械通气和循环稳定等; 非去极化肌松药(罗库溴铵、维库溴铵)的残留阻滞拮抗:使用胆碱酯酶抑制剂新斯的明。 | 新斯的明拮抗深度肌松时,通常用量很大,效果不佳,产生的副作用较大,罗库溴铵和维库溴铵引起的肌松残余,使用新斯的明后,残余肌松仍有20%和7%,临床上缺乏用于拮抗深度肌松的药物。
另外,新斯的明产生的副作用通常要求伍用抗胆碱药阿托品或格隆溴铵。 |
2008年以后:2008年首次在欧盟上市 销售,2010年FDA批准在美国上市, 2015年在日本上市,2017年在中国 批准上市。 | 去极化肌松药的残留阻滞拮抗:至今没有有效药物 非去极化肌松药(罗库溴铵、维库溴铵)的残留阻滞拮抗:新斯的明; 舒更葡糖钠。 | 舒更葡糖钠的上市使得临床上深肌松残留得到有效治疗,3min即可迅速逆转罗库溴铵的深度肌松阻滞作用,逆转效果迅速而显著,且副作用比新斯的明小;不用伍用抗胆碱药;
2013年《中华医学会麻醉学分会:肌肉松弛药合理应用的 专家共识》指出布瑞亭相比其他产品,副作用较小,在成人、儿童、老年人及肾功能衰竭患者,肺部或心脏疾病患者中,耐受性更好,推荐使用;
2014版《中国麻醉学指南与专家共识》中也指出布瑞亭能在3min内迅速逆转罗库咸的深肌松阻滞作用,明显降低术后肌松残余发生率,并能提高罗库溴铵临床使用的安全性;
2017版中国麻醉学指南与专家共识》中更强调了临床上使用深肌松的麻醉手术和必要性,并指定布瑞亭作为效逆转罗库溴铵引起的深肌松的使用药物。 |
2020以后 | 去极化肌松药的残留阻滞拮抗:至今没有有效药物 非去极化肌松药(罗库溴铵、维库溴铵)的残留阻滞拮抗:新斯的明; 舒更葡糖钠; Aom0498 | 布瑞亭在临床使用时仍存在一定的缺陷:如再箭毒化、过敏、出血,严重肾功能损伤不能使用,因为舒更葡糖钠-罗库溴铵的复合物65-97%通过肾脏排泄,肌酐清除率低于30ml/min的患者避免使用。
Aom0498就目前的临床研究,未发生再箭毒化,过敏和出血的副作用,安全性更好,随着布瑞亭的临床使用推广,和临床采用深肌松麻醉手术的增多,医生们逐渐对肌松残留危害加深理解,肌松拮抗剂的使用将会更加广泛。 |
参考文献:
1、《2017版中国麻醉学指南与专家共识》;
2、《2014版中国麻醉学指南与专家共识》
导读:进入2022年,连续3天,CDE官网发多条临床相关指导原则。针对这14条指导原则/指南,小编进行了汇总,快来看看吧!
《罕见疾病药物临床研发技术指导原则》
《预防抗肿瘤药物所致恶心呕吐药物临床试验设计指导原则(试行)》
《肾功能不全患者药代动力学研究技术指导原则(试行)》
《“临床风险管理计划”撰写指导原则(试行)》
《基于“三结合”注册审评证据体系下的沟通交流技术指导原则》
《个例安全性报告E2B(R3)区域实施指南》
《慢性丙型病毒性肝炎直接抗病毒药物临床试验技术指导原则》
《溃疡性结肠炎治疗药物临床试验技术指导原则》
《克罗恩病治疗药物临床试验技术指导原则》
《新药研发过程中食物影响研究技术指导原则》
《药物临床试验数据管理与统计分析计划指导原则》
《患者报告结局在药物临床研发中应用的指导原则(试行)》
《化学仿制药晶型研究技术指导原则(试行)》
《研究者手册中安全性参考信息撰写技术指导原则》
罕见疾病的单病种发病率极低,药物研发的难度远远超过常见多发疾病,因此罕见疾病药物的临床研发,除了应遵循一般药物的研发
规律以外,更应密切结合其自身疾病特点,在确保严谨科学的基础上,采用更为灵活的设计,以通过有限的患者数据,获得更加充分的科
学证据,满足获益与风险的评估,支持监管决策。为促进罕见疾病药物研发,在国家药品监督管理局的部署下,药审中心组织制定了《罕
见疾病药物临床研发技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管
〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告:
附件:罕见疾病药物临床研发技术指导原则
国家药监局药审中心
2021年12月31日
为鼓励新药研发,在国家药品监督管理局的部署下,药审中心组织制定了《预防抗肿瘤药物所致恶心呕吐药物临床试验设计指导原则
(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国
家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
附件:预防抗肿瘤药物所致恶心呕吐药物临床试验设计指导原则(试行)
国家药监局药审中心
2021年12月31号
肾功能不全患者药代动力学研究通常是创新药临床药理学研究的内容之一,研究结果是支持相应人群调整用法用量等问题决策的科学
依据。为提示申办者相关研究的总体考虑和数据分析等问题,药审中心组织制定了《肾功能不全患者药代动力学研究技术指导原则(试
行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药
品监督管理局审查同意,现予发布,自发布之日起施行。此前发布的指导原则如有与本指导原则不一致之处,以本指导原则为准。
特此通告。
附件:肾功能不全患者药代动力学研究技术指导原则(试行)
国家药监局药审中心
2021年12月29日
为鼓励新药研发,在国家药品监督管理局的部署下,药审中心组织制定了《“临床风险管理计划”撰写指导原则(试行)》(见附
件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局
审查同意,现予发布,自发布之日起施行。
特此通告。
附件:“临床风险管理计划”撰写指导原则(试行)
国家药监局药审中心
2021年12月27日
为推动构建中医药理论、人用经验和临床试验相结合的中药注册审评证据体系,指导在“三结合”审评证据体系下研发的中药新药提
出临床专业沟通交流申请,药审中心起草了《基于“三结合”注册审评证据体系下的沟通交流技术指导原则(征求意见稿)》,经中心内
部讨论并组织专家研讨,已形成征求意见稿。现在中心网站予以公示,以广泛听取各界意见和建议。我们诚挚地欢迎社会各界对征求意见
稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个月。
您的反馈意见请发到以下联系人的邮箱:
联系人:薛斐然,xuefr@cde.org.cn
侯晨晨,houchch@cde.org.cn
感谢您的参与和大力支持!
药品审评中心
2022年1月5日
为实施《个例安全性报告E2B(R3)区域实施指南》(以下简称区域实施指南),药审中心已完成对临床试验期间药物警戒系统升级改
造,已于2022年1月1日上线试运行。申请人应及时完成系统配置,并按照区域实施指南要求实施E2B(R3),时间不得晚于2022年7月1日。
区域字段测试要求:
一、原通过测试用户原通过测试用户需生成一份符合区域实施指南要求的XML格式的测试ICSR并发送至E2Btest@cde.org.cn,邮件主题
标明“申请E2B(R3)中国区域字段测试-企业名称”,正文提供申办者名称、企业的唯一识别ID(N.2.r.2)、列出所测试的具体区域字
段及允许值。
二、尚未通过测试用户
尚未通过测试用户需在符合《药物临床试验期间安全性数据快速报告标准和程序》相关要求的基础上,参照上述测试要求申请测试。
如有问题可发送电子邮件至:ywjjxtwt@cde.org.cn。
附件:个例安全性报告E2B(R3)区域实施指南.zip
国家药品监督管理局药品审评中心
2022年1月5日
为指导慢性丙型病毒性肝炎直接抗病毒药物科学研发和评价,提供可供参考的技术标准,药审中心制定了《慢性丙型病毒性肝炎直接
抗病毒药物临床试验技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管
〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
附件:慢性丙型病毒性肝炎直接抗病毒药物临床试验技术指导原则
国家药监局药审中心
2021年12月27日
为进一步规范和指导溃疡性结肠炎治疗药物临床试验,提供可参考的技术规范,在国家药品监督管理局的部署下,药审中心组织制
定了《溃疡性结肠炎治疗药物临床试验技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通
知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
附件:溃疡性结肠炎治疗药物临床试验技术指导原则
国家药监局药审中心
2021年12月27日
为进一步规范和指导克罗恩病治疗药物临床试验,提供可参考的技术规范,在国家药品监督管理局的部署下,药审中心组织制定了
《克罗恩病治疗药物临床试验技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监
综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
附件:克罗恩病治疗药物临床试验技术指导原则
国家药监局药审中心
2021年12月27日
为促进新药早期临床研发,引导药品研发企业合理规范地开展食物影响研究,进一步指导新药研发过程中食物影响研究的实施和评
价,药审中心组织起草了《新药研发过程中食物影响研究技术指导原则》。根据《国家药监局综合司关于印发药品技术指导原则发布程序
的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起执行。
特此通告。
附件:新药研发过程中食物影响研究技术指导原则
国家药监局药审中心
2021年12月27日
为了适应近年来临床试验数据管理与统计分析技术与方法的不断发展,配合ICH相关指导原则的落地和实施,药审中心组织修订了
2016年7月发布的《药物临床试验数据管理与统计分析的计划和报告指导原则》,形成了《药物临床试验数据管理与统计分析计划指导原
则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品
监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
附件:药物临床试验数据管理与统计分析计划指导原则
国家药监局药审中心
2021年12月27日
为鼓励以患者为中心的新药研发理念,科学合理的运用患者报告结局,药审中心组织制定了《患者报告结局在药物临床研发中应用的
指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要
求,经国家药品监督管理局审查同意,现予发布,自发布之日起实施。
特此通告。
附件:患者报告结局在药物临床研发中应用的指导原则(试行)
国家药监局药审中心
2021年12月27日
为规范和指导化学仿制药的晶型研究,在国家药品监督管理局的部署下,药审中心组织制定了《化学仿制药晶型研究技术指导原则
(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国
家药品监督管理局审查同意,现予发布,自发布之日起施行。
特此通告。
附件:化学仿制药晶型研究技术指导原则(试行)
国家药监局药审中心
2021年12月23日
为配合《药品注册管理办法》《药物警戒质量管理办法》的实施,规范申办者报告临床试验期间发生的可疑且非预期严重不良反应,
在国家药品监督管理局的部署下,药审中心组织制定了《研究者手册中安全性参考信息撰写技术指导原则》(见附件)。根据《国家药监
局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,
自发布之日起施行。
特此通告。
附件:研究者手册中安全性参考信息撰写技术指导原则
国家药监局药审中心
2021年12月23日
近些年抗肿瘤新药研发中有时会在传统首次人体试验之后(或当中)融合扩展队列研究,该研究具有快速招募和获得信息不断变化等特
点,为提示研发者此类研究设计和实施过程中的风险和挑战以及风险管理等问题,药审中心组织制定了《抗肿瘤药首次人体试验扩展队列研
究技术指导原则(试行)》。
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。
特此通告。
附件:抗肿瘤药首次人体试验扩展队列研究技术指导原则(试行)
国家药监局药审中心 2021年12月22日
临床单次和多次给药剂量递增药代动力学研究是创新药早期临床研究的重要内容,为支持药物临床安全有效剂量探索、确定给药方案等
提供重要依据。原国家食品药品监督管理局于2005年发布的《化学药物临床药代动力学研究技术指导原则》涉及相关内容,但距今已有16
年,为满足当前创新药研发的需要,药审中心组织制定了《化学药创新药临床单次和多次给药剂量递增药代动力学研究技术指导原则》
根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查
同意,现予发布,自发布之日起施行。上述2005年版指导原则如有与本指导原则不一致之处,以本指导原则为准。
特此通告。
国家药监局药审中心
2021年12月22日
考虑当前疫情防控要求,为进一步加强对申请人的技术指导和服务,加大创新研发支持力度,提高沟通交流的质量和效率,我中心对现
有沟通交流渠道的功能定位进行了梳理,申请人可基于咨询问题类别分别提交并选取合适的咨询通道,具体通知如下:
一、对于药物研发关键阶段重大问题,申请人可依据《药物研发与技术审评沟通交流管理办法》(2020年第48号)提出相应沟通交流
会议申请,经审评团队审核,需召开会议的,将通过视频会议方式召开;无需召开会议的,将在时限内通过申请人之窗进行书面反馈。当
前,审评资源依然相对不足,我中心将在保证按时限审评的前提下,协调组织审评资源进行沟通交流,提高会议召开频次,尽力满足申请人
的需求。
二、对于一般性技术问题,推荐申请人通过网络平台进行咨询,我中心将咨询按技术性和非技术性问题进行分类管理,技术类问题15个
工作日内予以答复,非技术性问题10个工作日内予以答复。
三、对于注册受理和审评业务的实时咨询,我中心根据疫情防控要求将每周三的公开日咨询调整为电话咨询,申请人可拨打电话进行实
时咨询,每周一、周三、周五,拨打010-85243528可进行审评业务咨询;周二、周四,拨打010-85242306可进行注册受理咨询。限于咨
询量巨大和人力资源有限等因素,常常存在难以拨入情形,推荐申请人通过网络平台进行一般性技术问题咨询,或通过联系邮箱进行问题咨
询。
四、对于在审评品种管理问题的咨询,申请人可与项目管理人进行电话或邮件联系,具体联系方式参见“官方网站-办事服务-关于审评-
项目管理人员公示”。对于在审注册申请,在无法及时与项目管理人取得联系时,可按《药审中心关于业务咨询服务联络方式的通知》进行
邮箱联系,我中心将在3个工作日内与该受理号申请表载明的联系人进行联系。
五、对于在审评品种,审评团队根据审评需要可能发起问询式沟通交流,请申请人保持通讯畅通并关注申请人之窗,及时按要求进行反
馈。(转自:国家药品监督管理局药品审评中心)
我委拟修订聚乙烯醇药用辅料标准,为确保标准的科学性、合理性和适用性,现将拟制定(修订)的药用辅料标准公示征求社会
各界意见(详见附件)。公示期自发布之日起3个月。请认真研核,若有异议,请及时来函提交反馈意见,并附相关说明、实验数据
和联系方式。相关单位来函需加盖公章,个人来函需本人签名,同时将电子版发送至指定邮箱。
联系人:陈蕾、康笑博
电话:010-67079566、67079620
电子邮箱:475@chp.org.cn
通信地址:北京市东城区法华南里11号楼 国家药典委员会办公室
邮编:100061
国家药典委员会
2022年03月11日